在一个固定容积的密闭容器中,充入等物质的量的X和Y,发生如下反应:X(g)+Y(g)?2Z(g),(正反应放热反应);下列说法正确的是( )
| A、当反应达到平衡后,若升高温度,容积内压强不变 | B、当反应达到平衡后,充入Z气体,达到新平衡时,X的体积分数不变,但X的浓度升高 | C、在一定温度下,容器中气体压强增大,但平衡不移动 | D、若向容器内通入少量X,压强增大,但平衡不移动 |
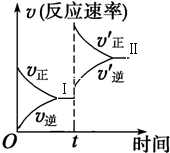 恒温密闭容器中,某反应的化学反应速率随时间变化关系如图所示,下列说法符合该图示的是( )
恒温密闭容器中,某反应的化学反应速率随时间变化关系如图所示,下列说法符合该图示的是( )| A、若平衡I到平衡II是由于改变温度造成的,则该反应为放热反应 | B、增大反应物的浓度,反应由平衡I变化到平衡Ⅱ | C、反应达到平衡I以后,减小反应物浓度,平衡移动到Ⅱ | D、反应达到平衡II时的化学反应速率比平衡I时的大 |
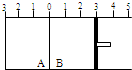 如图所示,温度不变时某容器分隔成A、B两部分,A、B容器之间的密封挡板可以左右自由移动,B容器右侧有可移动的活塞.现在A容器中充入2mol SO2和1mol O2,在B容器中充入2mol SO3(g)和1mol N2,在相同温度和压强下可发生可逆反应:2SO2(g)+O2(g)?2SO3(g).下列说法正确的是( )
如图所示,温度不变时某容器分隔成A、B两部分,A、B容器之间的密封挡板可以左右自由移动,B容器右侧有可移动的活塞.现在A容器中充入2mol SO2和1mol O2,在B容器中充入2mol SO3(g)和1mol N2,在相同温度和压强下可发生可逆反应:2SO2(g)+O2(g)?2SO3(g).下列说法正确的是( )| A、平衡后A、B两容器的体积相等 | B、平衡后A、B两容器中的SO3的体积分数相等 | C、平衡后A、B两容器中的SO2的转化率相等 | D、平衡后容器中SO2的物质的量:A<B |
一定温度下,1molX和nmol Y在容积为2L的密闭容器中发生如下反成:X(g)+Y(g)?2Z(g)+M(s),5min后达到平衡,此时生成2molZ.下列说法正确的是( )
| A、将容器压缩时,正逆反应速率均不变 | B、5 min内平均反应速率v(X)=0.2amol/(L?min) | C、向平衡后的体系中加入lmolM(s),平衡向逆反应方向移动 | D、当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
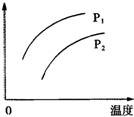 在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)=2C(g)△H>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示.则下列说法中,正确的是( )
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)=2C(g)△H>0,其他条件不变化,只有温度变化时,某量随温度变化的关系如图所示.则下列说法中,正确的是( )| A、若P1>P2,纵坐标表示A的质量分数 | B、若P1<P2,纵坐标表示C的质量分数 | C、若P1>P2,纵坐标表示混合气体的平均摩尔质量 | D、若P1<P2,纵坐标表示A的转化率 |
下列说法正确的是( )
| A、凡是放热反应都是自发的,吸热反应都是非自发的 | B、焓变小于0而熵变大于0的反应不一定是自发的 | C、增加反应物的浓度,可增多单位体积内活化分子数,从而使有效碰撞次数增多 | D、催化剂不影响反应活化能,但能增多单位体积内的活化分子数,从而增大反应速率 |
下列有关化学反应方向及其判据的说法中错误的是( )
| A、1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | B、△H<0的化学反应一定能自发进行 | C、CaCO3(s)?CaO(s)+CO2(g)△H>0 能否自发进行与温度有关 | D、△H<0,△S>0的反应一定是自发进行的化学反应 |
下列关于化学反应的自发性叙述中正确的是( )
| A、自发反应在恰当条件下才能实现 | B、焓变和熵变都小于0的反应肯定是自发的 | C、焓变和熵变都大于0的反应肯定是自发的 | D、自发反应一定是熵增大,非自发反应一定是熵减小 |
工业上可利用合成气(CO和H2的混合气体)生产甲醇.已知:CO(g)+2H2(g)?CH3OH(g)△H=-92.9kJ/mol 一定条件下,该反应在一体积固定的密闭容器中达到平衡.下列说法正确的是( )
| A、该反应的△S<0 | B、该反应在任何温度下均能自发进行 | C、向容器中充入少量He,平衡向正反应方向移动 | D、升高温度平衡向正反应方向移动 |
反应4NH3(气)+5O2(气)?4NO(气)+6H2O(气),在2L的密闭容器中进行,1分钟后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是( )
| A、NO:0.001摩/升 | B、H2O:0.002摩/升 | C、NH3:0.002摩/升 | D、O2:0.002摩/升 |