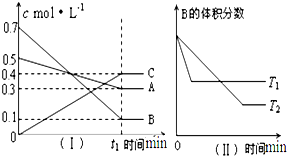
 T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1℃和T2℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论不正确的是( )
T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1℃和T2℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论不正确的是( )| A、在t1时间内用B表示该反应的平均速率为0.6/t1mol?L-1?min-1 | B、该反应的化学反应方程式为:A+3B?2C | C、其他条件不变,增大压强,正、逆反应速率均增大,气体的平均相对分子质量增大 | D、其他条件不变,温度由T1升高到T2,平衡时B的转化率降低 |
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)?NH3(g)+HI(g) ②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol?L-1,c(HI)=4mol?L-1,下列说法正确的是( )
①NH4I(s)?NH3(g)+HI(g) ②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol?L-1,c(HI)=4mol?L-1,下列说法正确的是( )
| A、平衡时,c(NH3)=6 mol?L-1 | B、反应起始时固体NH4I是5 mol | C、平衡时HI的分解率为20% | D、若改变反应起始固体NH4I的量,保持其他条件不变,平衡时各气体浓度也发生改变 |
已建立平衡的某可逆反应,当条件改变化学平衡正向移动时,下列叙述正确的是( )
①生成物的体积分数一定增大 ②生成物的产量一定增加
③生成物的产率一定增大 ④反应物浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥混合气体平均相对分子质量一定增大.
①生成物的体积分数一定增大 ②生成物的产量一定增加
③生成物的产率一定增大 ④反应物浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥混合气体平均相对分子质量一定增大.
| A、①②③ | B、①④⑤ | C、②⑤ | D、②④⑤ |
反应3A2(g)+B2(g)?2BA3(g)达到平衡时,不断改变反应条件(不改变A2、B2和BA3的量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中BA3的含量最高的一段时间是( )
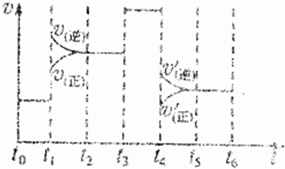

| A、t0-t1 | B、t2-t3 | C、t3-t4 | D、t5-t6 |
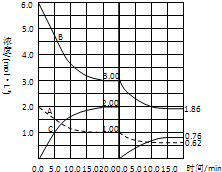 在恒容条件下发生反应A(g)+3B(g)
在恒容条件下发生反应A(g)+3B(g)| 催化剂 |
改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法中正确的是( )
| A、第Ⅰ阶段用C表示的平衡前的反应速率v (C)=0.1 mol/(L?S) |
| B、第Ⅱ阶段中B的平衡转化率αⅡ(B)为0.019 |
| C、第Ⅰ阶段的平衡常数KⅠ与第Ⅱ阶段平衡常数KⅡ的大小关系是:KⅠ<KⅡ |
| D、由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C |
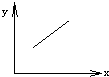 在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)(正反应为放热反应)达平衡后,改变一个条件(x),下列量(y)一定符合图中曲线所示变化的是( )
在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)(正反应为放热反应)达平衡后,改变一个条件(x),下列量(y)一定符合图中曲线所示变化的是( )