下列各组元素性质或原子结构的递变,叙述不正确的是( )
| A、Na、Mg、Al原子最外层电子数依次增多 | B、P、S、Cl元素最高正化合价依次增大 | C、N、O、F得电子能力依次减弱 | D、Li、Na、K的电子层数依次增多 |
砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )
| A、分子中共价键键角均为109°28′ | B、黄砷中共价键键能大于白磷 | C、黄砷分子极性大于白磷 | D、黄砷的熔点高于白磷 |
下列关于元素第一电离能的说法不正确的是( )
| A、外层电子排布为ns2np6(若只有K层时为1s2)的原子第一电离能较大 | B、对于同一元素而言,原子的I1<I2<I 3<I4… | C、同周期元素原子半径从左到右逐渐减小,故第一电离能必定依次增大 | D、钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
以下有关原子半径的叙述正确的是( )
| A、原子半径的大小取决于原子核外电子层数 | B、原子半径的大小取决于核电荷数 | C、同周期主族元素,原子半径随原子序数增大而增大 | D、同主族元素,原子半径随原子序数减小而减小 |
下列各组顺序的排列不正确的是( )
| A、酸性:H3PO4<H2SO4<HClO4 | B、热稳定性:HCl>H2S>PH3 | C、原子半径:Na<Mg<Al | D、氧化性:Cl2>Br2>I2 |
下列与有关非金属元素叙述以及推理结果不正确的是( )
①非金属性F>Cl,故将F2通入NaCl溶液中,发生反应为:F2+2Cl-=Cl2+2F-
②非金属性F>Br,故酸性:HF>HBr
③非金属性S>33As,故前者的气态氢化物稳定性更强
④非金属性O>N,故O2与H2化合比N2更容易.
①非金属性F>Cl,故将F2通入NaCl溶液中,发生反应为:F2+2Cl-=Cl2+2F-
②非金属性F>Br,故酸性:HF>HBr
③非金属性S>33As,故前者的气态氢化物稳定性更强
④非金属性O>N,故O2与H2化合比N2更容易.
| A、①② | B、③④ | C、①④ | D、②③ |
若把周期表原先的主、副族号取消,由左到右按原顺序编为18列.如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
| A、第3列元素种类最多,第14列元素形成化合物种类最多 | B、第10列元素全部是金属元素 | C、第18列元素单质全部是气体 | D、只有第2列元素的原子最外层有2个电子 |
下列各表为周期表的一部分(表中数字代表原子序数),正确的是( )
A、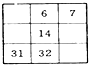 | B、 | C、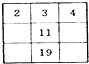 | D、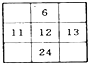 |