下列各种性质比较中,正确的是( )
| A、单质的熔点:K>Na>Li | B、熔点:金刚石>汞>氯化钠 | C、离子半径Al3+>Na+>Cl- | D、分子的稳定性:HF>H2O>NH3 |
X、Y、Z、W、R为原子序数递增的5种短周期元素,已知X的离子为一个质子,Y原子最外层电子数比内层电子数多4个,Y与R同主族,Z的最外层电子数等于其周期序数,W是制造太阳能电池的常用材料.下列说法正确的是( )
| A、原子半径按X、Y、Z、R、W依次递增 | B、Z与Y形成的化合物可作为耐火材料 | C、WY2能与强碱反应,但不能与任何酸反应 | D、热稳定性:X2R>X2Y |
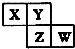 X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
| A、X、Y、Z的原子半径大小:X>Y>Z | B、X、W的气态氢化物能相互反应,生成共价化合物 | C、Z、W的最高价氧化物对应水化物的酸性,前者更强 | D、Y的单质与氢气反应较Z剧烈 |
X、Y是同周期的主族元素,且电负性大小:X>Y.下列说法错误的是( )
| A、X与Y形成的化合物中,X显负价,Y显正价 | B、第一电离能可能Y小于X | C、X的最高价含氧酸酸性弱于Y的 | D、气态氢化物的稳定性:HmY小于HnX |
元素X、Y、Z均为短周期元素且原子序数之和为35,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A、三种元素的原子序数 Y>X>Z | B、三种元素的原子半径 X>Y>Z | C、同周期元素中Y的金属性最强 | D、同周期元素中Y的最高价氧化物的水化物酸性最强 |
短周期主族元素A、B、C的原子序数依次递增,它们的族序数之和为11,A、C同主族,B原子最外层电子数比A原子次外层电子数多1.下列叙述正确的是( )
| A、原子半径:B>C>A | B、A、C两元素的最高价氧化物对应水化物的酸性A弱于C | C、B的最高价氧化物的水化物只能与酸反应,不能与碱反应 | D、B的最高价氧化物的熔点比A的最高价氧化物的熔点低 |
下列说法正确的是( )
| A、最外层电子数相同的元素一定处于同一主族 | B、能形成+2价阳离子的元素一定是ⅡA族元素 | C、在短周期元素中属于非金属元素的有12种 | D、在通常状况下,其单质有气态、液态、固态的族只有ⅦA族 |
某矿石由前20号元素中的四种组成,其化学式为WYZX4.X、Y、Z、W分布在三个周期,原子序数依次增大,Y、W为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同一周期,Z单质是一种良好的半导体.则下列判断正确的是( )
| A、Y、Z的氧化物都有两性 | B、气态氢化物的稳定性:Z>X | C、原子半径:W>Y>Z>X | D、最高价氧化物对应水化物的碱性:Y>W |
短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10.A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述正确的是( )
| A、D元素处于元素周期表中第3周期第IV族 | B、四种元素的原子半径:A<B<D<C | C、B、D的最高价氧化物中,B、D与氧原子之间均为双键 | D、一定条件下,B单质能置换出D单质,C单质能置换出A单质 |