下列各组元素的性质比较正确的是( )
| A、第一电离能:Li>Na>K | B、电负性:N>O>C | C、离子半径:Na+>Mg2+>S2->Cl- | D、原子半径:P>N>C |
下列电子排布图所表示的元素原子中,其能量处于最低状态的是( )
A、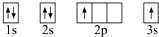 | B、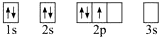 | C、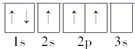 | D、 |
元素的化学性质主要决定于( )
| A、主要化合价 | B、核外电子数 | C、原子半径 | D、最外层电子数 |
下列数字为几种元素的核电荷数,其中原子的最外层电子数最多的是( )
| A、8 | B、14 | C、20 | D、33 |
下列各分子中,所有原子都满足最外层为8电子结构的是( )
| A、H2O | B、BF3 | C、CCl4 | D、PCl3 |
关于Si、P、S、Cl元素及化合物的有关说法正确的是( )
| A、原子半径依次增大,非金属性逐渐增强 | B、水泥、玻璃、水晶饰物都是硅酸盐制品 | C、含有Ag+等重金属离子的工业废水,通常用Na2S进行处理 | D、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
下列有关结构和性质的说法中,正确的是( )
| A、第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子 | B、同周期元素(除0族元素外)从左到右,原子半径逐渐减小 | C、第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 | D、NH3、HNO3都是电解质,二者反应后的产物是离子化合物,含极性共价键和离子键 |
X.Y是周期表前二十号元素,已知X.Y之间原子序数相差3,X.Y能形成化合物M.下列说法不正确的是
( )
( )
| A、若X.Y处于同一周期,则化合物M可能是正四面体型分子晶体 | B、若X的单质常温下是气体,则Y的单质常温下不可能是气体 | C、若X.Y两元素周期数差1,则属于离子化合物的M有四种 | D、若M属于离子晶体,则其中可能含有非极性键 |
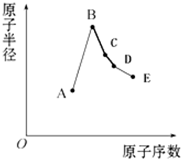 短周期元素中:A是地壳中含量最高的元素;B比Ne的质子数多1个;C最外层电子数与其电子层数相等;D单质是半导体材料;E非金属性在同周期元素中最强.下列说法中正确的是( )
短周期元素中:A是地壳中含量最高的元素;B比Ne的质子数多1个;C最外层电子数与其电子层数相等;D单质是半导体材料;E非金属性在同周期元素中最强.下列说法中正确的是( )| A、B离子的半径比C离子的半径小 | B、A、B两单质反应可得到两种不同的离子化合物 | C、C单质与A或E单质形成的化合物均为离子化合物 | D、B最高价氧化物对应的水合物与D单质发生反应能产生气体 |