高温及催化剂作用下,某反应的平衡常数K=
.恒容时,温度升高,H2浓度减小,下列说法正确的是( )
| [CO2][H2] |
| [CO][H2O] |
A、恒温下,将容器体积变为原来2倍,CO的平衡浓度变为原来的
| |||
| B、恒温恒容下,增大压强,H2浓度一定减小 | |||
| C、升高温度,正反应速率减小,逆反应速率增大 | |||
D、该反应化学方程式为CO2+H2
|
下列叙述中错误的是( )
| A、在平衡体系PCl5(g)?PCl3(g)+Cl2(g)中加入一定量的37Cl2,一段时间后37Cl存在于五氯化磷、三氯化磷和氯气这三种物质中 | B、CH3COOH与H18O-CH2CH3发生酯化反应是可逆反应,达到平衡后,18O仅存在于乙醇和乙酸乙酯分子里,不可能存在于乙酸和水分子里 | C、在氧气中完全燃烧后生成物只有CO2和H2O的有机物一定是烃 | D、CH2Cl2没有同分异构体的事实证明了甲烷分子是以碳原子为中心的正四面体结构 |
 已知反应3A(g)+B(g)?2C(g)+2D(g)△H<0,如图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况.若想使曲线b(实线)变为曲线a(虚线),可采用的措施是( )
已知反应3A(g)+B(g)?2C(g)+2D(g)△H<0,如图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况.若想使曲线b(实线)变为曲线a(虚线),可采用的措施是( )①增大A的浓度 ②升高温度 ③增大D浓度 ④加入催化剂 ⑤恒温下,缩小反应容器体积 ⑥加入稀有气体,保持容器内压强不变.
| A、①②③ | B、④⑤ | C、③④⑤ | D、④⑤⑥ |
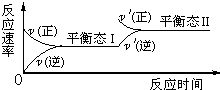 如图是恒温下某化学反应的反应速率随反应时间变化的示意图,下列叙述与示意图不相符合的是( )
如图是恒温下某化学反应的反应速率随反应时间变化的示意图,下列叙述与示意图不相符合的是( )| A、反应达平衡时,正反应速率和逆反应速率相等 | B、该反应达到平衡态 I后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ | C、该反应达到平衡态 I后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ | D、同一种反应物在平衡态 I和平衡态Ⅱ时浓度相等 |
在100℃时,将0.40molNO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
|