工业生产NH3、H2SO4过程中,有一些相似之处,它是( )
| A、都用到热交换器 | B、都需要高温高压 | C、都需要用催化剂 | D、都用到吸收塔 |
在Nd2O3等稀土催化剂的作用下可发生反应:4CO+2NO2
N2+4CO2,若该反应的反应速率分别用v(CO)、v(NO2)、v(N2)、v(CO2)表示,则下列关系中正确的是( )
| ||
. |
A、
| ||
B、
| ||
C、
| ||
D、
|
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.Ni(s)+4CO(g)
Ni(CO)4(g)△H<0,下列说法正确的是( )
| 50-80℃ |
| 180-200℃ |
| A、50~80℃时,适当增大压强,有利于Ni(CO)4的生成 | ||
| B、利用上述原理提纯粗镍需要消耗大量的CO气体 | ||
| C、50~200℃范围内,该反应的平衡常数随温度的升高而减小 | ||
D、该反应的平衡常数表达式是K=
|
下列事实不能用勒夏特勒原理解释的是( )
| A、热的纯碱溶液洗涤油污效果好 | B、饱和FeCl3溶液加热煮沸溶液呈红褐色 | C、醋酸溶液加水稀释,c(OH-)增大 | D、锌与稀硫酸反应,加入少量硫酸铜反应速率加快 |
一定量的稀H2SO4 与过量铁粉反应时,为减缓反应速率,且不影响生成H2的总量,可采取的措施是( )
| A、将铁粉改为铁片 | B、向稀H2SO4中加入少量的CuSO4溶液 | C、向稀H2SO4中加入少量的CH3COONa固体 | D、向稀H2SO4中加入少量的NaOH固体 |
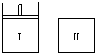 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器.其它条件相同时,在Ⅰ.Ⅱ中分别加入
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器.其它条件相同时,在Ⅰ.Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X.Y状态未知):2X(?)+Y(?)?aZ(g).此时Ⅰ中X.Y.Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
| A、若X为固态,Y为气态,则Ⅰ.Ⅱ中从起始到平衡所需时间相同 | B、若X.Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ | C、平衡时Ⅰ容器的体积小于VL | D、若X.Y均为气态,则平衡时气体平均摩尔质量:Ⅰ<Ⅱ |
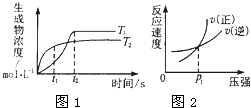 可逆反应aA(g)+bB(g)?c(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )
可逆反应aA(g)+bB(g)?c(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )| A、a+b>c+d T1<T2△H<0 | B、a+b>c+d T1<T2△H>0 | C、a+b<c+d T1>T2△H<0 | D、a+b>c+d T1>T2?H>0 |
下列事实中,不能用勒夏特列原理(平衡移动原理)解释的是 ( )
| A、合成氨工业上,采用高压以提高NH3的产率 | B、在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 | C、实验室中常用排饱和食盐水的方法收集Cl2 | D、工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |