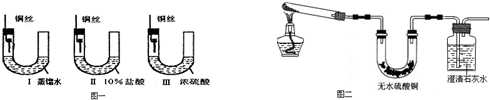
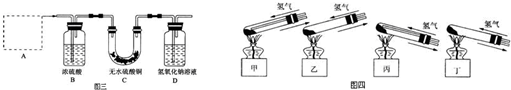
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.在纸内是离子“流过”水和氧化锌组成的电解液.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、电池正极反应式为:2MnO2+2e-+2H2O═2MnO(OH)+2OH- | B、该电池的正极为锌 | C、当0.1mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 | D、该电池反应中二氧化锰起催化作用 |
某种氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是( )
| A、负极反应式为:H2+2OH--2e-?2H2O | B、正极反应式为:O2+4H++4e-?2H2O | C、工作一段时间,KOH溶液的浓度不变 | D、电池工作时,电子由正极通过外电路流向负极 |
己知:2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
下列结论正确的是( )
| A、H2的燃烧热△H=-241.8kJ?mol-1 | B、炭和和水蒸气转化为水煤气为放热反应 | C、将24g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0kJ?mol-1 | D、1mol H2O(g)完全分解需要吸收241.8kJ热量 |
25℃,101k Pa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ/mol,辛烷和硫的燃烧热分别为5518kJ/mol和269kJ/mol.下列热化学方程式书写不正确的是( )
A、C8H18(g)+
| ||
| B、KOH(aq)+HNO3(aq)=KNO3(aq)+H2O(l);△H=-57.3kJ/mol | ||
| C、S(s)+O2(g)=SO2(g);△H=-269kJ/mol | ||
| D、2H+(aq)+SO42- (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1);△H=-114.6kJ/mol |
铅蓄电池的总反应方程式为:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O.下列说法正确的是( )
| 充电 |
| 放电 |
| A、放电时,负极的电极反应式是PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| B、充电时,电解液中H2SO4的浓度将变小 |
| C、放电时,转移l mol电子,参加反应的铅有0.5mol |
| D、充电时,蓄电池的负极和外接电源的正极相连 |
下列说法正确的是( )
| A、向盐酸中滴加氨水的离子方程式:H++OH-?H2O | B、强碱性溶液中大量存在:K+、Al3+、Cl-、SO42- | C、原电池的外电路中,电子由正极流向负极 | D、电解池的内电路中,阳离子向阴极移动 |
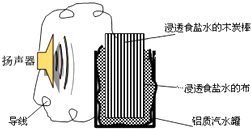 小明利用家中废旧材料制作了一个可使玩具扬声器发出声音的电池,装置如图.下列有关该电池工作时的说法错误的是( )
小明利用家中废旧材料制作了一个可使玩具扬声器发出声音的电池,装置如图.下列有关该电池工作时的说法错误的是( )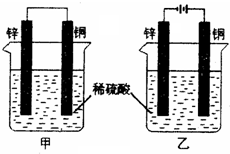 将纯锌片和纯铜片按如图所示方式插入同浓度的稀H2SO4中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按如图所示方式插入同浓度的稀H2SO4中一段时间,以下叙述正确的是( )