实验室用铅蓄电池进行电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极为Pb+S
?PbSO4+2e-,
正极为PbO2+4H++S
+2e-?PbSO4+2H2O,
今若制得Cl2 0.025mol,这时电池内消耗的H2SO4的物质的量至少是( )
负极为Pb+S
| O | 2- 4 |
正极为PbO2+4H++S
| O | 2- 4 |
今若制得Cl2 0.025mol,这时电池内消耗的H2SO4的物质的量至少是( )
| A、0.025 mol |
| B、0.050 mol |
| C、0.10 mol |
| D、0.20 mol |
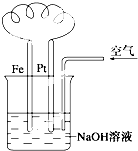 有关如图装置中的叙述正确的是( )
有关如图装置中的叙述正确的是( )| A、这是电解NaOH溶液的装置 | B、溶液中发生了变化:4Fe(OH)2+O2+2H2O?4Fe(OH)3 | C、Fe为正极,电极反应为:Fe-2e-+2OH-?Fe(OH)2 | D、NaOH溶液的碱性逐渐减弱 |
下列关于实验现象的描述不正确的是( )
| A、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 | B、用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌 | C、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
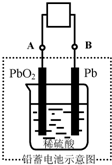 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为: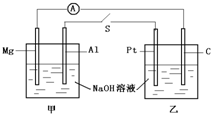 如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )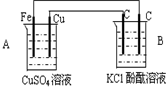 如图装置进行实验,关于此装置,下列的叙述正确的是( )
如图装置进行实验,关于此装置,下列的叙述正确的是( )