下列关于热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 | B、CO(g)的燃烧热是283.0 kJ?mol-1,则2CO2(g)?2CO(g)+O2(g)反应的△H=(2×283.0)kJ?mol-1 | C、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 | D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
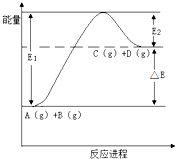 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )| A、该反应是放热反应 | B、加入催化剂后,反应加快,△E减小 | C、反应物的总键能大于生成物的总键能 | D、反应达到平衡时,升高温度,A的转化率增大 |
(1)已知胆矾失水的化学反应方程式为:CuSO4?5H2O(s)=CuSO4(s)+5H2O(l);△H=+Q1kJ/mol
(2)室温下,无水硫酸铜溶于水的热化学方程式为:
CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-Q2kJ/mol
(3)胆矾溶于水时,溶液温度降低.Q1与Q2的关系是(Q1、Q2为正数)( )
(2)室温下,无水硫酸铜溶于水的热化学方程式为:
CuSO4(s)=Cu2+(aq)+SO42-(aq);△H=-Q2kJ/mol
(3)胆矾溶于水时,溶液温度降低.Q1与Q2的关系是(Q1、Q2为正数)( )
| A、Q1>Q2 | B、Q1=Q2 | C、Q1<Q2 | D、无法确定 |
PS-Br储能电池的原理为(x+1)Na2Sx+Br2
xNa2Sx+1+2NaBr,下列有关该电池的说法中不正确的是( )
| 放电 |
| 充点 |
| A、电池充电时,阳极的电极反应式为2Br--2e-?Br2 |
| B、电池放电时,Na2Sx为负极 |
| C、电池充电时,电能转化为化学能 |
| D、电池放电时,Na+向负极移动 |
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应:
①Si(s)+3HCl(g)
SiHCl3(g)+H2(g)+381kJ
②SiHCl3(g)+H2(g)
Si(s)+3HCl(g)
对上述两个反应的叙述中,错误的是( )
①Si(s)+3HCl(g)
| 300℃ |
②SiHCl3(g)+H2(g)
| 1000-1100℃ |
对上述两个反应的叙述中,错误的是( )
| A、两个反应都是置换反应 |
| B、反应②是吸热反应 |
| C、两个反应互为可逆反应 |
| D、两个反应都是氧化还原反应 |
关于下列各装置图的叙述中,正确的是( )
A、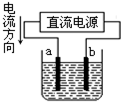 若采用该装置精炼铜,则a极为纯铜,b极为粗铜,电解质溶液为CuSO4溶液 | B、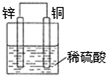 该装置是原电池,能将化学能转化为电能,锌电极发生还原反应 | C、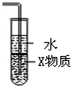 该装置中X若为四氯化碳,则此装置可用于吸收氨气,并防止倒吸 | D、 该装置可用于实验室配置一定物质的量浓度的稀硫酸 |
关于下列各图的分析或叙述,正确的是( )
A、 此图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ?mol-1 | B、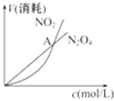 此图表示恒温恒容条件下,反应:2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | C、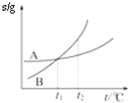 此图表示A、B两物质的溶解度随温度变化的情况,若将tl℃时A、B的饱和溶液分别升温至t2℃,则溶质的质量分数B>A | D、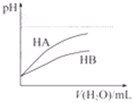 此图表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH |
下列说法正确的是( )
| A、中和热测定实验中,若用铜质搅拌器,则所测中和热的绝对值偏大 | B、用待测液润洗滴定用的锥形瓶,会使滴定结果偏低 | C、滴定终点读取滴定管刻度时,俯视标准液液面,会导致测定结果偏大 | D、配制一定物质的量浓度的溶液,定容时仰视刻度线,会使所配溶液浓度偏低 |
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO.其过程如下:
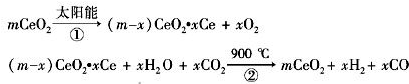
下列说法不正确的是( )
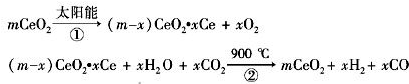
下列说法不正确的是( )
| A、该过程中CeO2没有消耗 | B、该过程实现了太阳能向化学能的转化 | C、右图中△H1=△H2+△H3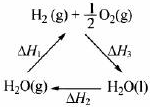 | D、以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-═CO32-+2H2O |
 一种碳纳米管能够吸附氢气,可做二次电池(如下图所示)的碳电极.该电池的电解质为6mol/L KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,可做二次电池(如下图所示)的碳电极.该电池的电解质为6mol/L KOH溶液,下列说法中正确的是( )