0 21145 21153 21159 21163 21169 21171 21175 21181 21183 21189 21195 21199 21201 21205 21211 21213 21219 21223 21225 21229 21231 21235 21237 21239 21240 21241 21243 21244 21245 21247 21249 21253 21255 21259 21261 21265 21271 21273 21279 21283 21285 21289 21295 21301 21303 21309 21313 21315 21321 21325 21331 21339 203614
 有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2
有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2  2SO3.则下列描述正确的是( )
2SO3.则下列描述正确的是( )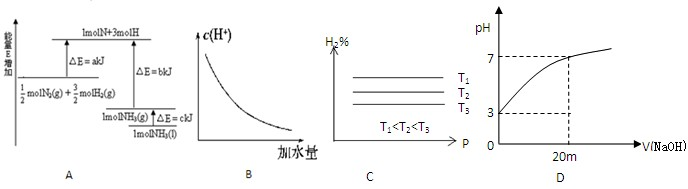
 H++F-,如只改变一个条件一定可以使c(HF)/c(H+)减小的是( )
H++F-,如只改变一个条件一定可以使c(HF)/c(H+)减小的是( )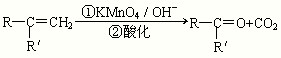 (R、R'可表示烃基或官能团)
(R、R'可表示烃基或官能团)

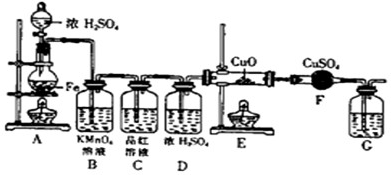

 Cr2O72-+H2O
Cr2O72-+H2O
 HSO3-+OH-
HSO3-+OH-