0 21097 21105 21111 21115 21121 21123 21127 21133 21135 21141 21147 21151 21153 21157 21163 21165 21171 21175 21177 21181 21183 21187 21189 21191 21192 21193 21195 21196 21197 21199 21201 21205 21207 21211 21213 21217 21223 21225 21231 21235 21237 21241 21247 21253 21255 21261 21265 21267 21273 21277 21283 21291 203614

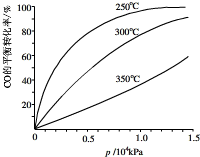 (2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.

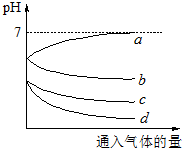 (2013?闵行区二模)向等体积等物质的量浓度的H2S和SO2的水溶液各两份中,分别通入不同的气体,一段时间后,如图表示通入的气体的量与溶液pH关系的曲线图,下列说法中正确的是( )
(2013?闵行区二模)向等体积等物质的量浓度的H2S和SO2的水溶液各两份中,分别通入不同的气体,一段时间后,如图表示通入的气体的量与溶液pH关系的曲线图,下列说法中正确的是( ) (2013?闵行区二模)用内置有螺旋状铜丝的胶头滴管小心吸取一滴管浓硝酸后迅速插入细口瓶中(如右图),滴管与瓶口接触处垫一小块滤纸使滴管与瓶口留少量空隙,依次观察到如下现象:①滴管内产生红棕色气体,液面下降;②滴管内液面上升,气体变成无色;③滴管内液面再次下降.下列说法中错误的是( )
(2013?闵行区二模)用内置有螺旋状铜丝的胶头滴管小心吸取一滴管浓硝酸后迅速插入细口瓶中(如右图),滴管与瓶口接触处垫一小块滤纸使滴管与瓶口留少量空隙,依次观察到如下现象:①滴管内产生红棕色气体,液面下降;②滴管内液面上升,气体变成无色;③滴管内液面再次下降.下列说法中错误的是( )