题目内容
 (2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.I.利用反应:6NO2+8NH3
| 催化剂 | △ |
II.一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)?SO3(g)+NO(g)-Q.
III.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)?CH3OH(g).
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2)=
0.015mol/(L?min)
0.015mol/(L?min)
.(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
bc
bc
(选填编号).a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(3)如果Ⅱ中反应的平衡常数K值变大,该反应
a
a
(选填编号).a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
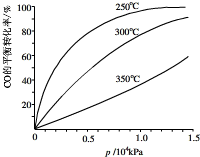
(4)对于Ⅲ中的反应,CO在不同温度下的平衡转化率与压强的关系如图示.该反应是
放热
放热
反应(填“放热”或“吸热”).实际生产条件控制在250℃、1.3×104kPa左右,简述选择此压强的理由:在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
.分析:(1)利用氧化还原反应中电子转移计算出参加反应的NO2,然后再根据速率公式进行计算;
(2)a.随反应:NO2(g)+SO2(g)?SO3(g)+NO(g)的进行,气体的总的物质的量不变,压强不变.
b.混合气体颜色保持不变,说明二氧化氮的浓度不变.
c.随反应进行NO2和SO3的体积之比发生变化.
d.反应前后气体的质量不变,物质的量也不变,所以平均相对分子质量保持不变;
(3)反应的平衡常数K值变大,只有改变温度使得平衡正向移动;
(4)由图示可知:相同压强下,温度升高,该反应CO的平衡转化率降低,说明平衡逆向移动,则正反应为放热反应;根据此时CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
(2)a.随反应:NO2(g)+SO2(g)?SO3(g)+NO(g)的进行,气体的总的物质的量不变,压强不变.
b.混合气体颜色保持不变,说明二氧化氮的浓度不变.
c.随反应进行NO2和SO3的体积之比发生变化.
d.反应前后气体的质量不变,物质的量也不变,所以平均相对分子质量保持不变;
(3)反应的平衡常数K值变大,只有改变温度使得平衡正向移动;
(4)由图示可知:相同压强下,温度升高,该反应CO的平衡转化率降低,说明平衡逆向移动,则正反应为放热反应;根据此时CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
解答:解:(1)对于6NO2+8NH3
7N2+12H2O,当有6molNO2反应共转移了24mol电子,所以电子转移了1.2mol,参加反应的NO2为0.3mol,则0~10min时,平均反应速率υ(NO2)=
=0.015mol/(L?min),
故答案为:0.015mol/(L?min);
(2)a.无论反应是否达到平衡状态,反应体系内的压强始终不变,所以不能根据“体系压强保持不变”判断反应是否达到平衡状态,故a错误;
b.当反应达到平衡状态时,二氧化氮的浓度不变,所以能根据“混合气体颜色保持不变”判断是否达到平衡状态,故b正确;
c.随反应进行NO2和SO3的体积之比发生变化.NO2和SO3的体积之比保持不变,说明到达平衡状态,故c正确;
d.反应前后气体的质量不变,物质的量也不变,所以平均相对分子质量保持不变,所以不能根据“混合气体的平均相对分子质量保持不变”判断反应是否达到平衡状态,故错误;
故选:bc;
(3)化学平衡常数只随温度的变化而变化,该反应为吸热反应,平衡常数K值变大说明温度升高平衡右移,正反应速率先增大后减小,逆反应速率先增大再增大,故a正确,故选:a;
(4)由图示可知:相同压强下,温度升高,该反应CO的平衡转化率降低,说明平衡逆向移动,则正反应为放热反应;根据此时CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失,
故答案为:放热;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
| 催化剂 |
| △ |
| ||
| 10min |
故答案为:0.015mol/(L?min);
(2)a.无论反应是否达到平衡状态,反应体系内的压强始终不变,所以不能根据“体系压强保持不变”判断反应是否达到平衡状态,故a错误;
b.当反应达到平衡状态时,二氧化氮的浓度不变,所以能根据“混合气体颜色保持不变”判断是否达到平衡状态,故b正确;
c.随反应进行NO2和SO3的体积之比发生变化.NO2和SO3的体积之比保持不变,说明到达平衡状态,故c正确;
d.反应前后气体的质量不变,物质的量也不变,所以平均相对分子质量保持不变,所以不能根据“混合气体的平均相对分子质量保持不变”判断反应是否达到平衡状态,故错误;
故选:bc;
(3)化学平衡常数只随温度的变化而变化,该反应为吸热反应,平衡常数K值变大说明温度升高平衡右移,正反应速率先增大后减小,逆反应速率先增大再增大,故a正确,故选:a;
(4)由图示可知:相同压强下,温度升高,该反应CO的平衡转化率降低,说明平衡逆向移动,则正反应为放热反应;根据此时CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失,
故答案为:放热;在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
点评:本题主要考查化学反应速率的计算、平衡状态判断、平衡常数、平衡移动,注意平时知识的积累以及灵活应用是解题的关键,难度不大.

练习册系列答案
相关题目

 R-CHO+HCHO
R-CHO+HCHO
 、
、
 为原料制备
为原料制备 的有关化学反应方程式(无机试剂任用).
的有关化学反应方程式(无机试剂任用). (2013?闵行区二模)2011年为国际化学年,也是为了纪念居里夫人发现放射性元素镭(Ra)并获得诺贝尔化
(2013?闵行区二模)2011年为国际化学年,也是为了纪念居里夫人发现放射性元素镭(Ra)并获得诺贝尔化