0 20478 20486 20492 20496 20502 20504 20508 20514 20516 20522 20528 20532 20534 20538 20544 20546 20552 20556 20558 20562 20564 20568 20570 20572 20573 20574 20576 20577 20578 20580 20582 20586 20588 20592 20594 20598 20604 20606 20612 20616 20618 20622 20628 20634 20636 20642 20646 20648 20654 20658 20664 20672 203614
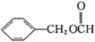
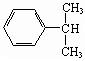
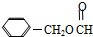 )是一种重要的工业使用的有机溶剂.分析如图的框图关系,然后回答问题:
)是一种重要的工业使用的有机溶剂.分析如图的框图关系,然后回答问题: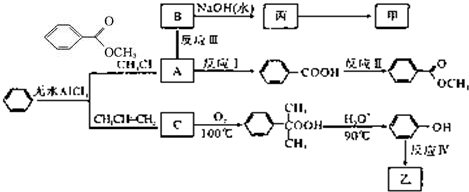
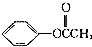
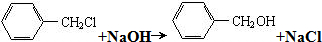
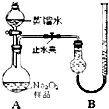 (2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.
(2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.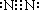
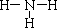
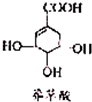 (2010?广州二模)莽草酸可用于合成甲型流感药物--达菲.下列关于莽草酸的叙述正确的是( )
(2010?广州二模)莽草酸可用于合成甲型流感药物--达菲.下列关于莽草酸的叙述正确的是( )