0 20318 20326 20332 20336 20342 20344 20348 20354 20356 20362 20368 20372 20374 20378 20384 20386 20392 20396 20398 20402 20404 20408 20410 20412 20413 20414 20416 20417 20418 20420 20422 20426 20428 20432 20434 20438 20444 20446 20452 20456 20458 20462 20468 20474 20476 20482 20486 20488 20494 20498 20504 20512 203614
 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.

 +CH3OH
+CH3OH
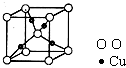 [化学--物质结构与性质]
[化学--物质结构与性质]

