0 20118 20126 20132 20136 20142 20144 20148 20154 20156 20162 20168 20172 20174 20178 20184 20186 20192 20196 20198 20202 20204 20208 20210 20212 20213 20214 20216 20217 20218 20220 20222 20226 20228 20232 20234 20238 20244 20246 20252 20256 20258 20262 20268 20274 20276 20282 20286 20288 20294 20298 20304 20312 203614
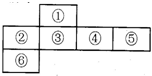 短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等