0 19203 19211 19217 19221 19227 19229 19233 19239 19241 19247 19253 19257 19259 19263 19269 19271 19277 19281 19283 19287 19289 19293 19295 19297 19298 19299 19301 19302 19303 19305 19307 19311 19313 19317 19319 19323 19329 19331 19337 19341 19343 19347 19353 19359 19361 19367 19371 19373 19379 19383 19389 19397 203614

 1,4-二甲苯
1,4-二甲苯 1,3,5-三甲苯
1,3,5-三甲苯
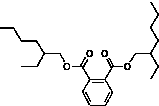 受台湾“塑化剂污染食品”风波的影响,2011年6月1日卫生部紧急发布公告,将塑化剂列入食品中可能违法添加的非食用物质和易滥用的食品添加剂名单.已知塑化剂DEHP分子结构简式如图.下列说法中不正确的是( )
受台湾“塑化剂污染食品”风波的影响,2011年6月1日卫生部紧急发布公告,将塑化剂列入食品中可能违法添加的非食用物质和易滥用的食品添加剂名单.已知塑化剂DEHP分子结构简式如图.下列说法中不正确的是( )