【题目】在蒸馏实验中,下列叙述不正确的是
A.在蒸馏烧瓶中加入约1/3体积的自来水,并放入几粒碎瓷片
B.蒸馏操作中,烧瓶可直接加热
C.冷水从冷凝管的下口入,上口出
D.收集冷凝水时,应弃去开始蒸馏出的部分
【题目】用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如下:
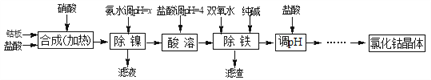
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
化学式 | 沉淀完全时的pH | 钴镍性质 |
Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
Fe(OH)2 | 9.6 | |
Fe (OH)3 | 3.7 |
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响见表中数据:从表中数据可知,当PH调节至x=_______时,除镍效果最好。
加NH3·H2O调pH | 收率/% | Ni2+含量/% |
9 | 98.1 | 0.08 |
9.5 | 98 | 0.05 |
10 | 97.6 | 0.005 |
10.3 | 94 | 0.005 |
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________________________。
(4)“除铁”步骤中加入的纯碱作用是_______________________________。
(5)在“调pH”步骤中,加盐酸的作用是______________________________。
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O![]() Fe(OH)3+3H+的平衡常数为_____________________。
Fe(OH)3+3H+的平衡常数为_____________________。
【题目】下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
元素 | 有关信息 |
A | 元素主要化合价为-2,原子半径为0.074nm |
B | 所在主族序数与所在周期序数之差为4 ,形成的单质是黄绿色有毒气体 |
C | 原子半径为 |
D | 最高价氧化物的水化物能按 |
E | 原子半径为 |
(1)写出C元素在周期表中的位置_________________,写出D元素最高价氧化物的水化物电子式________________。
(2)写出A与C元素气态氢化物的稳定性由大到小的顺序是______________![]() 填化学式
填化学式![]() 。
。
(3)写出B与C元素最高价氧化物的水化物酸性由弱到强的顺序是_________![]() 填化学式
填化学式![]() 。
。
(4)写出D的单质在氧气中燃烧生成产物为淡黄色固体,该氧化物含有的化学键类型是________________。
(5)砷![]() 与E同一主族,As原子比E原子多两个电子层,则As的原子序数为_______,其氢化物的化学式为___________。
与E同一主族,As原子比E原子多两个电子层,则As的原子序数为_______,其氢化物的化学式为___________。