【题目】过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为
CO(NH2)2+H2O2![]() CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
CO(NH2)2·H2O2 | 白色 晶体 | 45 ℃ | 75~85 ℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:
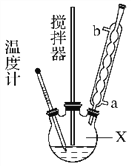
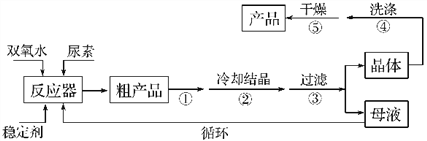
请回答下列问题:
(1)仪器X的名称是________;冷凝管中冷却水从________(填“a”或“b”)口出来。
(2)该反应的温度控制30 ℃而不能过高的原因是_____________________。
(3)步骤①宜采用的操作是________(填字母)。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是______________________________。
(5)准确称取1.000 g产品于250 mL锥形瓶中,加适量蒸馏水溶解,再加2 mL 6 mol·L-1H2SO4,用0.200 0 mol·L-1 KMnO4标准溶液滴定至终点时消耗18.00 mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”“偏低”或“不变”)。
【题目】半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)

已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;②PCl3遇水会强烈水解生 成 H3PO3和HC1;③PCl3遇O2会生成P0Cl3,P0Cl3溶于PCl3;④PCl3、POCl3的熔沸点见下表:
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | ﹣112 | 75.5 |
POCl3 | 2 | 105.3 |
请回答下列问题:
(1)A装置中制氯气的离子方程式为 ;
(2)F中碱石灰的作用是 、 ;
(3)实验时,检査装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是 ;
(4)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后.通过 (填实验操作名称),即可得到较纯净的PCl3;
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为 ;
(6)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000molL﹣1碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000molL﹣1的Na2S2O3,溶液滴定
③重复②、③操作,平均消耗Na2S2O3,溶液8.40ml
已知:H3PO3+H2O+I2═H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,假设测定过程中没有其他反应.根据上述数据,该产品中PC13的质量分数为 .