0 18056 18064 18070 18074 18080 18082 18086 18092 18094 18100 18106 18110 18112 18116 18122 18124 18130 18134 18136 18140 18142 18146 18148 18150 18151 18152 18154 18155 18156 18158 18160 18164 18166 18170 18172 18176 18182 18184 18190 18194 18196 18200 18206 18212 18214 18220 18224 18226 18232 18236 18242 18250 203614
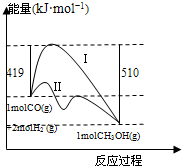 (2010?石家庄模拟)已知反应CO(g)+2H2(g)?CH3OH(g)的能量情况如图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
(2010?石家庄模拟)已知反应CO(g)+2H2(g)?CH3OH(g)的能量情况如图所示,曲线I和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
 (2012?许昌三模)[化学--选修3:物质结构与性质]砷(As)是一种重要的化学元素,其可形成多种用途广泛的化合物.
(2012?许昌三模)[化学--选修3:物质结构与性质]砷(As)是一种重要的化学元素,其可形成多种用途广泛的化合物.