题目内容
(2012?许昌三模)碳及其化合物的研究具有重要的现实意义.
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
请完成并配平上述化学方程式.
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).
下表所列数据是在不同温度下的化学平衡常数(K)
①在一定条件下将2mol CO和6mol H2充入2L的密闭容器中发生反应,5分钟后测得c(CO)=0.4mol/L,算此段时间的反应速率(用H2表示)
②由表中数据判断上述合成甲醇反应的△H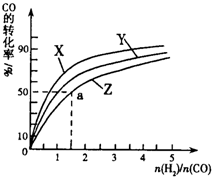
③在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系请回答:
(Ⅰ)在上述三种温度中,曲线Z对应的温度是
(Ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K=
④一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳.写出该电池负极发生反应的电极方程式
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为7×10-4 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
3
3
C+2
2
K2Cr2O7+8
8
H2SO4
H2SO4
→3
3
CO2↑+2
2
K2SO4+2
2
Cr2(SO4)3+8
8
H2O请完成并配平上述化学方程式.
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).
下表所列数据是在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.0 | 0.27 | 0.012 |
0.24
0.24
mol/(L?min);②由表中数据判断上述合成甲醇反应的△H
<
<
0(填“>”、“<”或“=”)
③在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系请回答:
(Ⅰ)在上述三种温度中,曲线Z对应的温度是
270℃
270℃
;(Ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K=
4L2?mol-2
4L2?mol-2
.④一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳.写出该电池负极发生反应的电极方程式
CH3OH+H2O═CO2+6H++6e-
CH3OH+H2O═CO2+6H++6e-
.(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为7×10-4 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为
1.6×10-5mol/L
1.6×10-5mol/L
.分析:(1)反应中C元素的化合价由0升高为+4价,Cr元素的化合价由+6价降低为+3价,结合化合价升降总数相等以及质量守恒定律配平;
(2)①依据化学反应的三段式列式计算;
②平衡常数随温度变化,温度升高K减小说明温度升高平衡左移,逆向是吸热反应,正向是放热反应;
③(Ⅰ)根据该反应为放热反应,温度越高CO的转化率越小,所以曲线Z为270℃;
(Ⅱ)根据平衡常数表达式和一氧化碳的转化率求算;
④燃料电池中,负极上甲醇失电子发生氧化反应,生成二氧化碳;
(3)Na2CO3溶液的浓度为7×10-4mol/L,等体积混合后溶液中c(CO32-)=7×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍.
(2)①依据化学反应的三段式列式计算;
②平衡常数随温度变化,温度升高K减小说明温度升高平衡左移,逆向是吸热反应,正向是放热反应;
③(Ⅰ)根据该反应为放热反应,温度越高CO的转化率越小,所以曲线Z为270℃;
(Ⅱ)根据平衡常数表达式和一氧化碳的转化率求算;
④燃料电池中,负极上甲醇失电子发生氧化反应,生成二氧化碳;
(3)Na2CO3溶液的浓度为7×10-4mol/L,等体积混合后溶液中c(CO32-)=7×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍.
解答:解:(1)反应中C元素的化合价由0升高为+4价,一个碳化合价变化4,Cr元素的化合价由+6价降低为+3价,1个K2Cr2O7化合价变化6,4和6的最小公倍数为12,由化合价升降总数相等可知,C的化学计量数为3,K2Cr2O7的化学计量数为2,由于产物中有Cr2(SO4)3,所以未知的反应物为H2SO4,最后由质量守恒定律可知得化学反应为3C+2K2Cr2O7+8H2SO4═3CO2+2K2SO4+2Cr2(SO4)3+8H2O,
故答案为:3;2;8;H2SO4;3;2;2;8;
(2)①依据化学平衡三段式列式得到
CO(g)+2H2(g)?CH3OH(g)
起始量(mol) 2 6 0
变化量(mol) x 2x x
5分钟量(mol) 2-x 6-2x x
5分钟后测得c(CO)=0.4mol/L,
所以2-x=0.4mol/L×2L,
所以x=1.2mol,
所以△c(H2)=1.2mol/L,
用H2表达的反应速率=
=0.24mol/(L?min),
故答案为:0.24;
②表中数据分析可知随温度升高,平衡常数K减小,说明温度升高,平衡逆向进行,所以正向是放热反应,△H<0,
故答案为:<;
③(Ⅰ)根据该反应为放热反应,温度越高CO的转化率越小,所以曲线Z为270℃,
故答案为:270℃;
(Ⅱ)②该反应的平衡常数K=
,初始时CO为2mol,H2为3mol;
a点时,CO转化率50%,反应消耗了2mol×50%=1molCO,消耗氢气2mol,剩余1molCO,n(H2)=3mol-2mol=1mol,生成1mol甲醇,
a点各组分的浓度是:c(CH3OH)=0.5mol/L,c(CO)=0.5mol/L,c(H2)=0.5mol/L,
带入表达式得:K=
=4L2?mol-2,
故答案是:4L2?mol-2;
④电极上燃料失电子发生氧化反应,该燃料电池的电解质溶液呈酸性,所以负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为:CH3OH-6e-+H2O═CO2+6H+,
故答案为:CH3OH-6e-+H2O═CO2+6H+;
(3)Na2CO3溶液的浓度为7×10-4mol/L,等体积混合后溶液中c(CO32-)=
×7×10-4mol/L=3.5×10-4mol/L,
根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,
c(Ca2+)=
mol/L=0.8×10-5mol/L,
原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,
故原溶液CaCl2溶液的最小浓度为2×0.8×10-5mol/L=1.6×10-5mol/L,
故答案为:1.6×10-5mol/L.
故答案为:3;2;8;H2SO4;3;2;2;8;
(2)①依据化学平衡三段式列式得到
CO(g)+2H2(g)?CH3OH(g)
起始量(mol) 2 6 0
变化量(mol) x 2x x
5分钟量(mol) 2-x 6-2x x
5分钟后测得c(CO)=0.4mol/L,
所以2-x=0.4mol/L×2L,
所以x=1.2mol,
所以△c(H2)=1.2mol/L,
用H2表达的反应速率=
| 1.2mol/L |
| 5min |
故答案为:0.24;
②表中数据分析可知随温度升高,平衡常数K减小,说明温度升高,平衡逆向进行,所以正向是放热反应,△H<0,
故答案为:<;
③(Ⅰ)根据该反应为放热反应,温度越高CO的转化率越小,所以曲线Z为270℃,
故答案为:270℃;
(Ⅱ)②该反应的平衡常数K=
| c(CH3OH) |
| c(CO)?c2(H2 ) |
a点时,CO转化率50%,反应消耗了2mol×50%=1molCO,消耗氢气2mol,剩余1molCO,n(H2)=3mol-2mol=1mol,生成1mol甲醇,
a点各组分的浓度是:c(CH3OH)=0.5mol/L,c(CO)=0.5mol/L,c(H2)=0.5mol/L,
带入表达式得:K=
| 0.5mol?L-1 |
| 0.5mol?L-1×(0.5mol?L-1)2 |
故答案是:4L2?mol-2;
④电极上燃料失电子发生氧化反应,该燃料电池的电解质溶液呈酸性,所以负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为:CH3OH-6e-+H2O═CO2+6H+,
故答案为:CH3OH-6e-+H2O═CO2+6H+;
(3)Na2CO3溶液的浓度为7×10-4mol/L,等体积混合后溶液中c(CO32-)=
| 1 |
| 2 |
根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,
c(Ca2+)=
| 2.8×10-9 |
| 3.5×10-4 |
原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,
故原溶液CaCl2溶液的最小浓度为2×0.8×10-5mol/L=1.6×10-5mol/L,
故答案为:1.6×10-5mol/L.
点评:本题考查了氧化还原反应的配平,反应速率的计算,反应平衡常数的计算、原电池原理,溶度积常数的应用,本题难度中等.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目