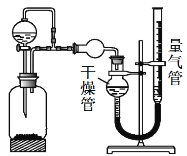
【题目】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按图所示工艺流程进行生产,可制得轻质氧化镁(轻质体积蓬松,体积是等质量的重质氧化镁的三倍)。

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表l 生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.l |
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。表2原料价格表
物质 | 价格/元 吨-1 |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
(1)为了加快卤块的溶解,我们可以选择那些方法_______(请写出两种方法);
(2)在步骤②中加入的试剂X,最佳的选择是________,在酸性条件下,其对应的离子方程式是________________
(3)在步骤③中加入的试剂应是________;之所以要控制pH=9.8,其目的是__________
(4)在步骤④中加入的试剂Z应是___________;
(5)在步骤⑤中发生的反应是__________
【题目】在固定容积为2L的密闭容器中,800℃时,发生反应2NO(g)+O2(g)![]() 2NO2(g), n(NO)随时间的变化如下表:
2NO2(g), n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
N(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
下列说法错误的是
A. 若使用合适的正催化剂反应到达平衡的时间少于3s
B. 0 ~2 s内O2的平均反应速率为0.003mol/(L·s)
C. 反应到第5s时,NO的转化率为65%
D. 3s后气体的颜色不再发生改变