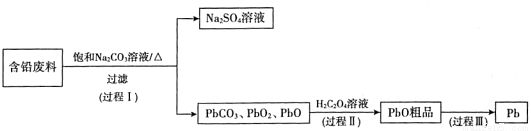
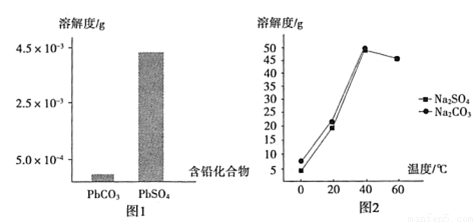
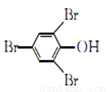
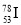将CH4、CO2催化重整为可用的化学品,对缓解能源危机、改善环境意义重大。

(l)以Fe(OH)3为脱硫剂,通过复分解反应吸收H2S,产物是H2O和___________。
(2)过程A主要涉及以下反应:
i. CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
ii. CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ/mol
CO2(g)+H2(g) △H=-41kJ/mol
①反应i的化学平衡常数K随温度的变化关系是____。
②分析反应iixt反应i中CO2转化率可能的影响并说明理由:____(写出一种即可)。
(3)某科研团队利用Ni、CaO、Fe3O4三种催化剂在850℃下“超干重整”CH4和CO2;
过程I.通入CO2和CH4,所得CO被吸收,H2O被分离出体系,如下面左图所示。
过程Ⅱ.H2O被分离后,向该装置中再通入He气,使催化剂再生并获得CO,如下面右图所示。

①CH4和CO2重整为CO、H2O的热化学方程式是____________。
②结合反应方程式简述Fe3O4的催化作用:___________。
③CaO对Fe3O4是否起到催化作用至关重要,实验研究结果如下表:
编号 | 催化剂 | 是否添加CaO | 还原产物 |
1 | Fe3O4 | 添加 | 有Fe |
2 | Fe3O4 | 不添加 | 无Fe |
运用有关化学原理解释实验结果:____。
某学生探究如下实验(A):
实验A | 条件 | 现象 |
| 加热 | i.加热后蓝色褪去 ii.冷却过程中,溶液恢复蓝色 ⅲ.一段时间后,蓝色重又褪去 |
(1)使淀粉变蓝的物质是____。
(2)分析现象i、ii认为:在酸性条件下,加热促进淀粉水解,冷却后平衡逆向移动。
设计实验如下,“现象a”证实该分析不合理:
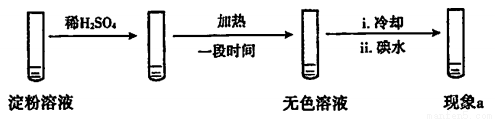
“现象a”是____。
(3)再次分析:加热后单质碘发生了变化,实验如下:
I:取少量碘水,加热至褪色,用淀粉溶液检验挥发出的物质,变蓝。
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷却过程中一直未变蓝;加入稀H2SO4,瞬间变蓝。
对步骤Ⅱ中稀H2SO4的作用,结合离子方程式,提出一种合理的解释:______________。
(4)探究碘水褪色后溶液的成分:
实验1:测得溶液的pH≈5
实验2:取褪色后的溶液,完成如下实验:
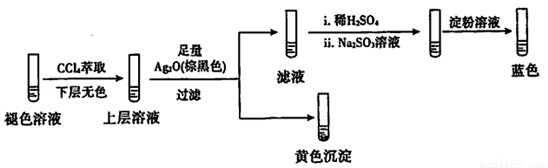
①产生黄色沉淀的离子方程式是____。
②Ag2O的作用是____________。
③依据上述实验,推测滤液中含有的物质(或离子)可能是_________。
(5)结合化学反应速率解释实验A中现象i、现象iii蓝色褪去的原因:_______________。

 2Fe2++I2
2Fe2++I2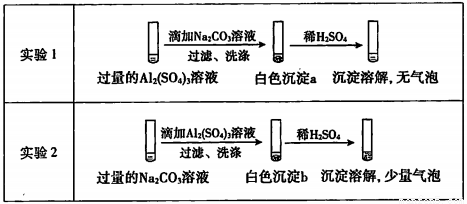
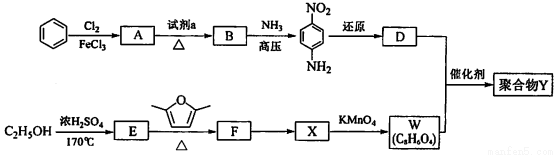
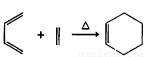
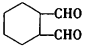 ,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。