0 17447 17455 17461 17465 17471 17473 17477 17483 17485 17491 17497 17501 17503 17507 17513 17515 17521 17525 17527 17531 17533 17537 17539 17541 17542 17543 17545 17546 17547 17549 17551 17555 17557 17561 17563 17567 17573 17575 17581 17585 17587 17591 17597 17603 17605 17611 17615 17617 17623 17627 17633 17641 203614
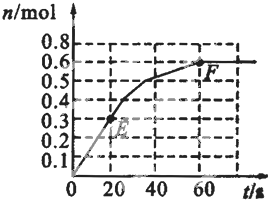 373K时,某1L密闭容器中发生如下可逆反应:A (g)?2B (g).其中物质B的物质的量变化如图所示
373K时,某1L密闭容器中发生如下可逆反应:A (g)?2B (g).其中物质B的物质的量变化如图所示