Ⅰ.烟道气中含有的CO和SO2是重要的污染物,可在催化剂作用下将它们转化为S(s)和CO2,此反应的热化学方程 式为_____________________。
式为_____________________。
 已知:CO(g) +1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1;
已知:CO(g) +1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1;
S(s)+O2=SO2(g) △H=-296.0 kJ·mol-1
Ⅱ.氨的合成是最重要的化工 生产之一。在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g)
生产之一。在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g) 2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
容 器 | 甲 | 乙 |
反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 |
达到平衡的时间(min) | t | 5 |
平衡时N2的浓度(mol·L-1) | 3 | c |
(1)该反应的平衡常数表达式K=_______________。
(2)甲容器达到平衡所需要的时间t 5min(填“>”、“<” 或“=”);
Ⅲ.下表是不同温度下水的离子积数据:
温度/℃ | 25 | t1 | t2 |
Kw/ mol2·L-2 | 1×10-14 | a | 1×10-12 |
试回答以下几个问题:
(1)若25< t1< t2,则a________1×10-14(填“<”、“>”或“=”)。
(2)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH—)为:____________mol/L。
(3)在t2℃下,将pH=9的氢氧化钠溶液V1 L与pH=4的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1︰V2 = ___________
某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60[ |
4 | 820℃ | 1.0 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
根据上述实验数据,完成下列填空:
(1)在实验1中,反应在10至20min时间内,反应物A的平均速率为 mol/(L·min)。
(2)在实验2中,A的初始浓度C2= mol/L,反应经20minA的浓度就不再发生变化,进而可推测实验2中隐含的条件是 。
(3)在实验3中,A的初始浓度C3 1.0mol/L(填>、=、<)。
(4)比较实验4和实验1,可推测该反应是____________反应(选填“吸热”、“放热”)。理由是_________________________。
 反应使之褪色的是
反应使之褪色的是 与氨水混合后,溶液pH=7
与氨水混合后,溶液pH=7
 工原料,受热易分解。某兴趣小组拟探究其分解产物。
工原料,受热易分解。某兴趣小组拟探究其分解产物。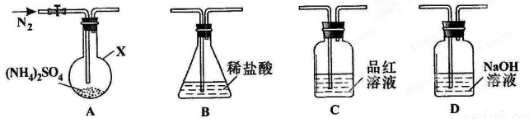
 液中无SO42-。
液中无SO42-。 到重要作用。
到重要作用。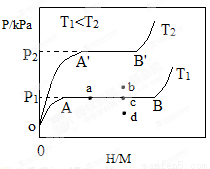
 合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MH与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)
合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MH与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g) zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。
zMHy(s) △H1(I);B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。 方式释放氢气。η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)___ _______η(T2)(填“>”“<”或“=”)。
方式释放氢气。η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)___ _______η(T2)(填“>”“<”或“=”)。