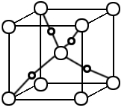
已知:常温下浓度为0.1mol/L的下列溶液的pH如表:
溶质 | NaCl | Na2CO3 | NaClO | NaHCO3 |
pH | 7 | 11.6 | 9.7 | 8.3 |
下列有关说法不 正确的是
正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力:HCl>H2CO3>HClO
B.等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl->ClO-[
C.向Na2CO3溶液中逐滴滴入少量稀盐酸,反应为:Na2CO3+2HCl=2NaCl+CO2↑+H2O
D.若将CO2通入0.1mol/L Na2CO3溶液至溶液中性,则溶液中:
2c(CO32-)+c(HCO3-)= 0.2mol/L
钛合金烤瓷牙是目前国内使用最为普遍的一种烤瓷牙,TiCl4是生产金属钛的原料。
(1)工业上主要用TiO2氯化的方法来制取TiCl4
① 有人拟用以下氯化反应来制取TiCl4:TiO2(s)+2Cl2(g) TiCl4(l)+O2(g) ,写出实验室用二氧化锰与浓盐酸反应制取Cl2的离子方程式 。
TiCl4(l)+O2(g) ,写出实验室用二氧化锰与浓盐酸反应制取Cl2的离子方程式 。
② 工业上通常往TiO2和Cl2反应体系中加入碳单质,在一定条件下制取TiCl4,从化学平衡的角度解释此方法能顺利制取TiCl4的原因 。
(2)某化学实验小组以TiO2和足量 CCl4为原料制取TiCl4,装置图如下:
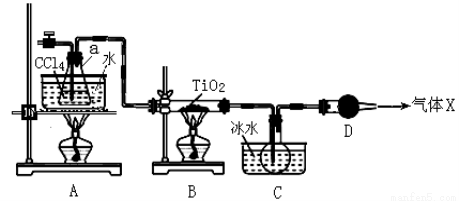
下表是有关物质的性质:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | ﹣23 | 76.8 | 与TiCl4互溶 |
TiCl4 | ﹣25 | 136 | 遇潮湿空气产生白雾 |
① 实验开始时先点燃A处的酒精灯,待C中烧瓶里有液滴出现时再点燃B处的酒精灯,其主要目的是 。
② 本实验中仪器a采用题给的加热方式的突出优点是 。
③ B中CCl4与TiO2发生反应的化学方程式是 。
④ 欲分离C装置中的TiCl4,应采用的实验操作为 (填操作名称)。
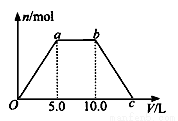
⑤ 若将反应过程中生成的气体X(足 量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图所示,若混合溶液中Ba( OH)2和2NaOH的物质的量之比为1:1,则b点溶液中溶质主要成分的化学式为 , 从b点到c点,沉淀减少过程中发生反应的离子方程式为 。
量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图所示,若混合溶液中Ba( OH)2和2NaOH的物质的量之比为1:1,则b点溶液中溶质主要成分的化学式为 , 从b点到c点,沉淀减少过程中发生反应的离子方程式为 。
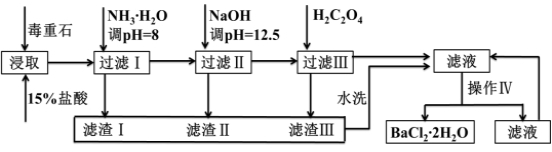
毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2?2H2O的流程如下:
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH |
| 9.1 | 1.9[ |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)= 1.6×10–7,Ksp(CaC2O4)= 2.3×10–9
(1)实验室用37%的盐酸配制1mol/L盐酸,下列仪器中,不需要使用的是_______ __
a.容量瓶 b.量筒  c.烧杯 d.滴定管
c.烧杯 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有______________(至少两条)。
(2)加入氨水调节溶液pH=8的目的是___________________________。滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是___ __ ____________。
(3)操作Ⅳ的步骤是:______ ______、过滤。
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O ;Ba2++CrO42— =BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点 ,测得滴加盐酸体积为V0 mL。
,测得滴加盐酸体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
通过计算,氯化钡溶液浓度为___________mol·L-1(用含字母的式子表示)。
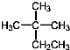 的系统命名为2﹣甲基﹣2﹣乙基丙烷
的系统命名为2﹣甲基﹣2﹣乙基丙烷 双键
双键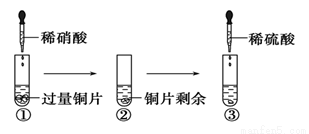
 CH3OH(g) ΔH =_______kJ·mol-1。
CH3OH(g) ΔH =_______kJ·mol-1。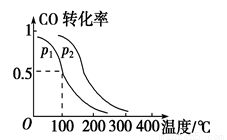
 11.9
11.9
 上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。 核外电子排布图:
核外电子排布图: ,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。 色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。