17.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5 mol1,3-丁二烯分子中含有C=C双键数为NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
14.下列有关实验的操作或判断正确的是 ( )
| A. | 取少量浑浊的天然水,加入适量明矾,天然水变得澄清透明 | |
| B. | 分别通过盛有品红溶液的洗气瓶可以鉴别SO2和CO2 | |
| C. | 保存硅酸钠溶液可以使用磨口玻璃塞、细口玻璃瓶 | |
| D. | 向Fe(OH)3胶体中逐滴加入过量的稀盐酸,先生成红褐色沉淀,最后沉淀又溶解 | |
| E. | 用镊子从煤油中夹取小块金属钠直接投入水中 |
13.如图是某加碘食盐包装袋上的部分图表文字.由此你得到的信息和作出的推测是( )
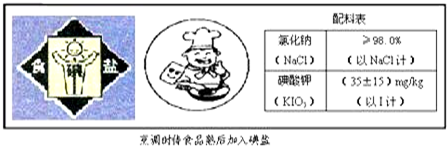

| A. | 可以用酒精从该碘盐配制的溶液中萃取KIO3 | |
| B. | “烹调时待食品熟后加入碘盐”的原因可能是碘酸钾受热易分解 | |
| C. | 1 kg此食盐中含碘酸钾(35±15)mg | |
| D. | 食用加碘盐的目的是预防龋齿 |
10.N、O、Si、S、Al、Fe、Cu是常见的七种元素.
(1)Si位于元素周期表第三周期第IVA族.
(2)Cu原子的价层电子排布图为 .
.
(3)基态Fe原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5.可用硫氰化钾检验Fe3+,形成的配合物的颜色为血红色.
(4)用“>”或“<”填空:
(5)氢元素和上述非元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为sp3;分子中既含有极性共价键、又含有非极性共价键的化合物是H2O2 或N2H4(填化学式,任写一种).
(6)O和Cu形成的一种离子化合物的晶体结构如图,则铜离子的电荷为+1.
(1)Si位于元素周期表第三周期第IVA族.
(2)Cu原子的价层电子排布图为
 .
.(3)基态Fe原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d5.可用硫氰化钾检验Fe3+,形成的配合物的颜色为血红色.
(4)用“>”或“<”填空:
| 离子半径 | 电负性 | 熔点 | 酸性 |
| O2-> Na+ | F>O | 金刚石> 晶体硅 | H2SO4<HClO4 |
(6)O和Cu形成的一种离子化合物的晶体结构如图,则铜离子的电荷为+1.

9.下列解释实验现象的反应方程式正确的是( )
0 173952 173960 173966 173970 173976 173978 173982 173988 173990 173996 174002 174006 174008 174012 174018 174020 174026 174030 174032 174036 174038 174042 174044 174046 174047 174048 174050 174051 174052 174054 174056 174060 174062 174066 174068 174072 174078 174080 174086 174090 174092 174096 174102 174108 174110 174116 174120 174122 174128 174132 174138 174146 203614
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2═Na2O2 | |
| B. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 向NaHCO3溶液中加入足量Ba(OH)2溶液,出现白色沉淀:2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O |

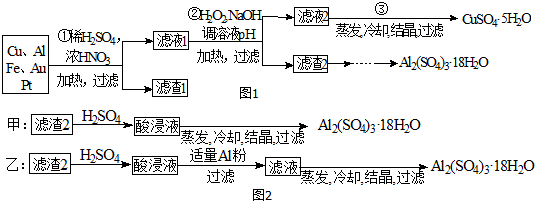
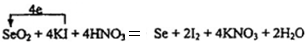 .
.