题目内容
9.下列解释实验现象的反应方程式正确的是( )| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2═Na2O2 | |
| B. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 向NaHCO3溶液中加入足量Ba(OH)2溶液,出现白色沉淀:2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O |
分析 A.不符合反应客观事实,钠与氧气常温下生成氧化钠;
B.不符合反应客观事实,二者反应生成氢氧化铝和氯化铵;
C.过氧化钠与水反应生成氢氧化钠和氧气;
D.向NaHCO3溶液中加入足量Ba(OH)2溶液,反应生成碳酸钡、氢氧化钠和水.
解答 解:A.切开的金属Na暴露在空气中,光亮表面逐渐变暗,离子方程式:4Na+O2═2Na2O,故A错误;
B.AlCl3溶液中加入过量稀氨水,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物,离子方程式:2Na2O2+2H2O═4NaOH+O2↑,故C正确;
D.向NaHCO3溶液中加入足量Ba(OH)2溶液,出现白色沉淀,离子方程式:HCO3-+Ba2++2H-═BaCO3↓+H2O,故D错误;
故选C.
点评 本题考查了离子方程式的书写,明确发生反应的实质及离子方程式书写方法是解题关键,注意反应物用量、反应条件对反应的影响,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
19.下列各物质中互为同系物的是( )
| A. | 甲醇、乙二醇 | B. | 正丁烷和异丁烷 | C. |  和 和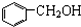 | D. |  和 和 |
20.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L酒精含有的分子数为 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.01 NA | |
| C. | 11.2 L H2所含的电子数为NA | |
| D. | 通常状况下,NA个CO2分子含有电子数为22 NA |
17.下列物质不属于高分子材料的是( )
| A. | 蛋白质 | B. | 纤维素 | C. | 淀粉 | D. | 油脂 |
14.下列有关实验的操作或判断正确的是 ( )
| A. | 取少量浑浊的天然水,加入适量明矾,天然水变得澄清透明 | |
| B. | 分别通过盛有品红溶液的洗气瓶可以鉴别SO2和CO2 | |
| C. | 保存硅酸钠溶液可以使用磨口玻璃塞、细口玻璃瓶 | |
| D. | 向Fe(OH)3胶体中逐滴加入过量的稀盐酸,先生成红褐色沉淀,最后沉淀又溶解 | |
| E. | 用镊子从煤油中夹取小块金属钠直接投入水中 |
1.对于反应2SO2(g)+O2(g)═2SO3(g),能增大逆反应速率的措施是( )
| A. | 移去部分O2 | B. | 增大容器体积 | C. | 移去部分SO3 | D. | 升高体系温度 |
18.A和B两种有机物可以互溶,其有关性质如表所示:
(1)要除去A、B混合物中的少量A,可采用A方法即可得到B.
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)若B的分子式为C2H6O,核磁共振氢谱表明其分子中有三种不同化学环境的氢原子,强度之比为3:2:1.则B的结构简式为CH3CH2OH.
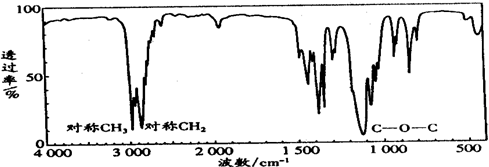
(3)若质谱图显示A的相对分子质量为74,红外光谱如图所示,则A的结构简式为CH3CH2OCH2CH3.
| C)°密度(20 | 熔点 | 沸点 | 熔解性 | |
| A | 0.713 7g•cm3- | C°-116.3 | C°34.5 | 不溶于水 |
| B | 0.789 3g•cm3- | C°-117.3 | C°78.5 | 与水以任意比混溶 |

(1)要除去A、B混合物中的少量A,可采用A方法即可得到B.
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)若B的分子式为C2H6O,核磁共振氢谱表明其分子中有三种不同化学环境的氢原子,强度之比为3:2:1.则B的结构简式为CH3CH2OH.
(3)若质谱图显示A的相对分子质量为74,红外光谱如图所示,则A的结构简式为CH3CH2OCH2CH3.

 .
.