13.某烃的相对分子质量为70,该烃能使溴的CCl4溶液褪色则该烃的结构最多有(不考虑立体异构)( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 4种 |
11.已知在CH4中,C-H键间的键角为109°28′,NH3中N-H键间的键角为107°.H2O中O-H键间的键角为105°,则下列说法中正确的是( )
| A. | 孤电子对与成键电子对间的斥力大于成键电子对间的斥力 | |
| B. | 孤电子对与成键电子对间的斥力小于成键电子对间的斥力 | |
| C. | 孤电子对与成键电子对间的斥力等于成键电子对与成键电子对间的斥力 | |
| D. | 题干中的数据不能说明孤电子对与成键电子对间的斥力与成键电子对与成键电子对间的斥力之间的大小关系 |
9.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
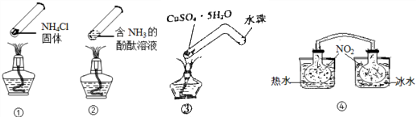

| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl易升华 | |
| B. | 加热时,②溶液颜色变,冷却后又恢复为原来的颜色 | |
| C. | 加热时,③中固体由蓝色变为白色,冷却后又恢复为原来的颜色 | |
| D. | ④中,浸泡在热水中的容器内气体颜色变深,说明受热时反应2NO2?N2O4向正方向移动 |
8.根据下列化学方程式:①2FeCl3+2KI=2FeCl2+I2+2KCl
②6FeCl3+3Br2=2FeBr3+4FeC13.
分析有关离子的还原性由弱到强的顺序是( )
②6FeCl3+3Br2=2FeBr3+4FeC13.
分析有关离子的还原性由弱到强的顺序是( )
| A. | Br-<Fe2+<I- | B. | I-<Fe2+<Br- | C. | Br-<I-<Fe2+ | D. | Fe2+<Br-<I- |
7.下列说法正确的是( )
| A. | 同温下,等物质的量浓度的A12(SO4)3比MgSO4溶液的pH小,说明镁比铝的金属性强 | |
| B. | 向Na2SiO3溶液中滴人酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失.证明非金属性:C1>Si | |
| C. | 测定等物质的量浓度的Na2CO3和Na2SiO3溶液的pH,确定碳、硅两元素非金属性的强弱 | |
| D. | 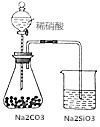 如图锥形瓶中有气体产生,烧杯中液体变浑浊,可证明N、C、Si非金属性依次减弱 如图锥形瓶中有气体产生,烧杯中液体变浑浊,可证明N、C、Si非金属性依次减弱 |
6. 如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
 如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )| A. | 关闭分液漏斗的活塞.将干燥管末端放人水中,微热烧瓶,有气泡从水中冒出,停止加热后,燥管内有水柱形成,表明装置不漏气 | |
| B. | 若装置用于制取氯气并验证其具有漂白性,则A中所用试剂为稀盐酸,B中所用药品为KMnO4固体,C中为品红溶液 | |
| C. | 若装置用于制取SO2并验证其具有漂白性,则A中所用试剂为浓硫酸,B中所用药品为Na2SO3固体,C中为酸性KMnO4溶液 | |
| D. | 若实验时B中盛放固体NaOH,A中为浓氨水,C中为稀AgNO3溶液,则实验过程中,C试管中看不到明显的实验现象 |
5.今有两种正盐的稀溶液,分别是a mol•L-1NaX溶液和b mol•L-1NaY溶液,下列说法正确的是( )
0 173804 173812 173818 173822 173828 173830 173834 173840 173842 173848 173854 173858 173860 173864 173870 173872 173878 173882 173884 173888 173890 173894 173896 173898 173899 173900 173902 173903 173904 173906 173908 173912 173914 173918 173920 173924 173930 173932 173938 173942 173944 173948 173954 173960 173962 173968 173972 173974 173980 173984 173990 173998 203614
| A. | 若a=b,pH(NaX)>pH(NaY),则酸性:HX>HY | |
| B. | 若a=b,并测得c(X-)=c(HY)+c(Y-),则HX是强酸 | |
| C. | 若a>b,c(X-)=c(Y-),可推出酸性:HX>HY | |
| D. | 若两溶液等体积混合,测得c(X-)+c(HX)+c(HY)+c(Y-)=0.1mol•L-1,则可求得a=b=0.1 |