4.在危险化学品的外包装标签上印有警示性标志.下列化学品名称与警示性标志名称对应不正确的是( )
| A. | 烧碱---剧毒品 | B. | 汽油---易燃品 | C. | 浓硫酸---腐蚀品 | D. | 酒精---易燃品 |
2.硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):

部分物质的物理性质如下表:
(l)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为素周期表的位置为第四周期、ⅥA族;H2SeO4的酸性比H2SO4的酸性弱(填“强”或“弱”).
(2)实验中往往需将硒鼓回收料粉碎,其目的是增大煅烧时与氧气的接触面积,加快反应速率,提高原料的利用率
(3)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量Te02杂质,除杂时适宜采用的方法是升华.
(4)以SO2为还原剂可将Se02还原为单质硒,写出反应的化学方程式:2SO2+Se02=Se+2SO3.

部分物质的物理性质如下表:
| 物理性质 | 熔点 | 沸点 | 溶解性 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
(2)实验中往往需将硒鼓回收料粉碎,其目的是增大煅烧时与氧气的接触面积,加快反应速率,提高原料的利用率
(3)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量Te02杂质,除杂时适宜采用的方法是升华.
(4)以SO2为还原剂可将Se02还原为单质硒,写出反应的化学方程式:2SO2+Se02=Se+2SO3.
19.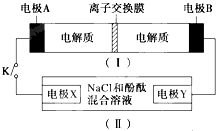 如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
 如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 闭合K时,K十从左到右通过离子交换膜 | |
| B. | 闭合K时,A的电极反应式为:3I--2e-═I2- | |
| C. | 闭合K时,X的电极反应式为:2CI--2e-═Cl2↑个 | |
| D. | 闭合K时,当有0.1mo1K+通过离子交换膜,X电极上产生标准状况下气体2.24L |
18.将充有m mol NO和n mol NO2气体的试管倒立于水槽中,然后通入m mol O2,若已知n>m,则充分反应后,试管中的气体在同温同压下的体积为( )
| A. | $\frac{4n-1}{2}$ | B. | $\frac{n-m}{3}$ | C. | $\frac{3m+n}{3}$ | D. | 3(n-m) |
17.a mol金属单质M和含2.5a mol HNO3的稀溶液恰好完全反应,氧化产物是M(NO3)2,则还原产物可能是( )
0 173783 173791 173797 173801 173807 173809 173813 173819 173821 173827 173833 173837 173839 173843 173849 173851 173857 173861 173863 173867 173869 173873 173875 173877 173878 173879 173881 173882 173883 173885 173887 173891 173893 173897 173899 173903 173909 173911 173917 173921 173923 173927 173933 173939 173941 173947 173951 173953 173959 173963 173969 173977 203614
| A. | NO2 | B. | NO | C. | N2O5 | D. | NH4NO3 |