14.下列说法中,错误的是( )
| A. | 纤维素的水解难于淀粉的水解 | |
| B. | 碘化钾溶液能使淀粉变蓝 | |
| C. | 多糖一般没有还原性,不能发生银镜反应 | |
| D. | 用淀粉制酒精仅发生了水解反应 |
10.实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液.
(2)容量瓶上需标有以下五项中的①③⑤.
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是BCAFED(用字母表示,每个字母只能用一次).
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,溶液注入容量瓶前需恢复到室温,这是因为容量瓶盛放热溶液时,体积不准.
(5)下列配制的溶液浓度偏小的是ABEF.
A.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
B.加蒸馏水时不慎超过了刻度线、
C.定容时俯视刻度线
D.配制前,容量瓶中有少量蒸馏水.
E.称量NaOH时,砝码错放在左盘
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水.
(1)配制250mL 1.25mol/L的NaOH溶液.
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外,还需要的其它玻璃仪器 |
| 12.5g | 250mL | 烧杯、玻璃棒、胶头滴管 |
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是BCAFED(用字母表示,每个字母只能用一次).
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面最低处恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是保证溶质全部转入容量瓶,溶液注入容量瓶前需恢复到室温,这是因为容量瓶盛放热溶液时,体积不准.
(5)下列配制的溶液浓度偏小的是ABEF.
A.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
B.加蒸馏水时不慎超过了刻度线、
C.定容时俯视刻度线
D.配制前,容量瓶中有少量蒸馏水.
E.称量NaOH时,砝码错放在左盘
F.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水.
9.反应I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$常用于精盐中碘含量测定.
(1)某同学利用该反应探究浓度对反应速率的影响.实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择②③④(填序号).
①1mL 0.01mol•L-1的碘水 ②1mL 0.001mol•L-1的碘水 ③4mL 0.01mol•L-1的Na2S2O3溶液 ④4mL 0.001mol•L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O${\;}_{3}^{2-}$)=8.33×10-4mol/(L•s).
(3)所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,200℃时,该反应的平衡常数为$\frac{1}{2.25}$,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol
•L-1)变化如表:
①请计算5min时H2O的平衡浓度0.006mol/L.
②CO的平衡转化率为40%.
③若5min~10min只改变了某一条件,该条件是增大水蒸气的浓度,如何改变的增大0.01mol/L.
(1)某同学利用该反应探究浓度对反应速率的影响.实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择②③④(填序号).
①1mL 0.01mol•L-1的碘水 ②1mL 0.001mol•L-1的碘水 ③4mL 0.01mol•L-1的Na2S2O3溶液 ④4mL 0.001mol•L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O${\;}_{3}^{2-}$)=8.33×10-4mol/(L•s).
(3)所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,200℃时,该反应的平衡常数为$\frac{1}{2.25}$,该温度下,将一定量的CO和H2投入某10L密闭容器,5min时达平衡,各物质浓度(mol
•L-1)变化如表:
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
②CO的平衡转化率为40%.
③若5min~10min只改变了某一条件,该条件是增大水蒸气的浓度,如何改变的增大0.01mol/L.
6.下列对原子结构的叙述正确的是( )
| A. | 1904年,道尔顿提出了一个被称为“葡萄干面包式”的原子结构模型 | |
| B. | 在化学反应过程中,原子最外层电子数不发生变化,但原子核可能会发生变化 | |
| C. | 在活泼金属与活泼非金属的反应中,金属元素的原子得到电子,表现为负化合价 | |
| D. | 原子不带电,原子的质量主要集中在原子核上 |
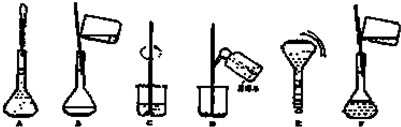
5.以下离子检验正确的是( )
0 173778 173786 173792 173796 173802 173804 173808 173814 173816 173822 173828 173832 173834 173838 173844 173846 173852 173856 173858 173862 173864 173868 173870 173872 173873 173874 173876 173877 173878 173880 173882 173886 173888 173892 173894 173898 173904 173906 173912 173916 173918 173922 173928 173934 173936 173942 173946 173948 173954 173958 173964 173972 203614
| A. | 检验试液中的SO42-:试液$\stackrel{BaCl_{2}溶液}{→}$ 白色沉淀$\stackrel{HCl溶液}{→}$ 白色沉淀 | |
| B. | 检验试液中的Cl-:试液$\stackrel{稀H_{2}SO_{4}}{→}$无沉淀$\stackrel{AgNO_{3}溶液}{→}$ 白色沉淀 | |
| C. | 检验试液中的Fe2+:试液$\stackrel{氯水}{→}$无明显现象$\stackrel{KSCN溶液}{→}$血红色溶液 | |
| D. | 检验试液中的NH4+:试液$→_{供热}^{NaOH溶液}$气体逸出$→_{石蕊试纸}^{湿润的红色}$ 试纸变蓝 |
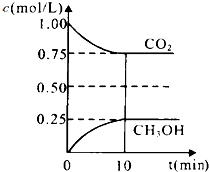 碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式.在一定温度下的2L固定容积的密闭容器中,通入2molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)CH3OH(g)+H2O(g),△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示. SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2$?_{△}^{催化剂}$2SO3.请回答下列问题:
SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2$?_{△}^{催化剂}$2SO3.请回答下列问题: