8.下列说法正确的是( )
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,0.5molN2和1.5molH2置于密闭容器中充分反应生成氨气,放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 在100℃、101kPa条件下,液态水的气化热为40.69kJ•mol-1,则H2O(g)?H2O(l) 的△H=+40.69 kJ•mol-1 | |
| D. | 酸碱发生中和反应生成1mol液态H2O时,所放出的热量称为中和热,可表示为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1 |
7.下列各组离子在指定溶液中能大量共存的是( )
| A. | 饱和氯水中:Cl?、NO${\;}_{3}^{-}$、Na+、SO${\;}_{3}^{2-}$ | |
| B. | Na2S溶液中:SO42-、K+、Cl?、Cu2+ | |
| C. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| D. | FeCl3溶液中:K+、NH4+、I-、SCN- |
6.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 标准状况下,22.4LSO3含有NASO3个分子 | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 常温常压下,0.1molCl2溶于水,转移的电子数目为0.1NA |
5.下列化学反应的离子方程式正确的是( )
| A. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | |
| C. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| D. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O |
1.一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)?H2(g)+I2(g).若[HI]由0.1mol•L-1降到0.07mol•L-1时,需要15s,那么[HI]由0.07mol•L-1降到0.05mol•L-1时,所需反应的时间为( )
0 173648 173656 173662 173666 173672 173674 173678 173684 173686 173692 173698 173702 173704 173708 173714 173716 173722 173726 173728 173732 173734 173738 173740 173742 173743 173744 173746 173747 173748 173750 173752 173756 173758 173762 173764 173768 173774 173776 173782 173786 173788 173792 173798 173804 173806 173812 173816 173818 173824 173828 173834 173842 203614
| A. | 等于5 s | B. | 等于10 s | C. | 大于10 s | D. | 小于10 s |
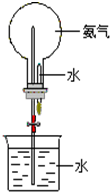 已知氨气与氯化氢气体都是极易溶于水的气体,在标准状况下1升水中最多能溶解500升的氯化氢气体,或者700升的氨气.
已知氨气与氯化氢气体都是极易溶于水的气体,在标准状况下1升水中最多能溶解500升的氯化氢气体,或者700升的氨气.