10.己知A(g)+B(g)?C(g)+D(g)反应的平衡常数和温度的关系如下表,则( )
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005mol/(L.s).下列说法正确的是( )
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A. | 4s时c(B)为0.76mol/L | |
| B. | 830℃达平衡时,A的转化率为80% | |
| C. | 反应达平衡后,升高温度,平衡正向移动 | |
| D. | 1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为0.4 |
4.催化剂能加快反应速率,下面关于催化剂的说法正确的是( )
| A. | 催化剂只改变正反应速率的速率 | |
| B. | 催化剂能够改变反应的反应热 | |
| C. | 催化剂能改变反应物的转化率 | |
| D. | 催化剂通过降低反应的活化能来加快反应速率 |
3.下列说法正确的是( )
| A. | 摩尔是物质的数量单位 | |
| B. | 58.5 gNaCl溶解在1 L水中,得到溶液的物质的量浓度为1mol/L | |
| C. | 标况下,1 mol CCl4 所占的体积约为22.4 L | |
| D. | 12g12C含有的碳原子数约为6.02×1023个 |
2.FeCl3溶液是化学实验室的常用试剂.
(1)某小组同学配制1.0mol/LFeCl3溶液的过程是:称取270.5gFeCl3•6H2O晶体,溶解于加了20mL浓盐酸的适量水中,稀释至1L.
则:配制过程中所需的玻璃仪器除烧杯、容量瓶外还有玻璃棒、胶头滴管、量筒.1.0mol/LFeCl3溶液的密度为1.12g/cm3,该溶液中含FeCl3的质量分数为14.5%.
(2)将1.0mol/L(NH4)2CO3溶液加到1.0mol/LFeCl3溶液中也可制得Fe(OH)3胶体,反应的化学方程式为3(NH4)2CO3+2FeCl3+3H2O=2Fe(OH)3(胶体)+3CO2↑+6NH4Cl.验证制得的分散系是胶体的方法是用一束光线照射制得的分散系,可以观察到一条光亮的“通路”(或丁达尔效应).
(3)取少量1.0mol/LFeCl3溶液加水稀释成0.1mol/L FeCl3溶液.
提示:KSCN中S元素的化合价为-2价.
①结合实验ⅰ、ⅱ分析,实验ⅰ中红色褪去的原因是SCN-被H2O2溶液氧化为SO42-,使溶液红色褪去.
②阅资料得知:Cl-对溶液红色褪去的反应有催化作用,验证该说法应补充的实验及现象是分别取2mL0.1mol/LFeCl3溶液和2mL0.05mol/LFe2(SO4)3溶液,分别滴入KSCN溶液,溶液均变为红色,再分别加入等浓度等体积的H2O2溶液,FeCl3溶液褪色快.
0 173536 173544 173550 173554 173560 173562 173566 173572 173574 173580 173586 173590 173592 173596 173602 173604 173610 173614 173616 173620 173622 173626 173628 173630 173631 173632 173634 173635 173636 173638 173640 173644 173646 173650 173652 173656 173662 173664 173670 173674 173676 173680 173686 173692 173694 173700 173704 173706 173712 173716 173722 173730 203614
(1)某小组同学配制1.0mol/LFeCl3溶液的过程是:称取270.5gFeCl3•6H2O晶体,溶解于加了20mL浓盐酸的适量水中,稀释至1L.
则:配制过程中所需的玻璃仪器除烧杯、容量瓶外还有玻璃棒、胶头滴管、量筒.1.0mol/LFeCl3溶液的密度为1.12g/cm3,该溶液中含FeCl3的质量分数为14.5%.
(2)将1.0mol/L(NH4)2CO3溶液加到1.0mol/LFeCl3溶液中也可制得Fe(OH)3胶体,反应的化学方程式为3(NH4)2CO3+2FeCl3+3H2O=2Fe(OH)3(胶体)+3CO2↑+6NH4Cl.验证制得的分散系是胶体的方法是用一束光线照射制得的分散系,可以观察到一条光亮的“通路”(或丁达尔效应).
(3)取少量1.0mol/LFeCl3溶液加水稀释成0.1mol/L FeCl3溶液.
| 实验序号 | 操作及现象 |
| ⅰ | 取2mL 0.1mol/L FeCl3溶液,滴入3滴0.1mol/L KSCN溶液,溶液变为红色,通入一段时间O2,无明显变化.再加入3滴 1mol/L H2O2溶液,红色很快褪去. |
| ⅱ | 取少量ⅰ中所得溶液滴加入BaCl2溶液,产生白色沉淀,加入盐酸,沉淀不溶解. |
①结合实验ⅰ、ⅱ分析,实验ⅰ中红色褪去的原因是SCN-被H2O2溶液氧化为SO42-,使溶液红色褪去.
②阅资料得知:Cl-对溶液红色褪去的反应有催化作用,验证该说法应补充的实验及现象是分别取2mL0.1mol/LFeCl3溶液和2mL0.05mol/LFe2(SO4)3溶液,分别滴入KSCN溶液,溶液均变为红色,再分别加入等浓度等体积的H2O2溶液,FeCl3溶液褪色快.
 某同学配制98mL 3.0mol•L-1 NaOH溶液的实验步骤如下:
某同学配制98mL 3.0mol•L-1 NaOH溶液的实验步骤如下: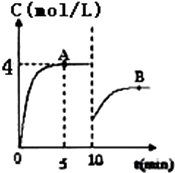 在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol•L-1和b mol•L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图所示.
在一定条件下,合成塔中氮气和氢气的起始浓度分别为a mol•L-1和b mol•L-1,反应为:N2+3H2?2NH3,氨气的浓度随时间变化如图所示.