8.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,22.4 L 14CO2与44 g 14CO2含分子数均为NA | |
| B. | 1 mol CH3COOH与足量CH3CH2OH在浓硫酸存在下共热生成NA个乙酸乙酯分子 | |
| C. | 常温下,pH=13的NaOH溶液中含OH-离子数为0.1 NA | |
| D. | 浓度为2 mol/L的FeCl3溶液500 mL水解后生成Fe(OH)3胶体粒子数目小于NA |
7.下列实验操作或结论正确的是( )
| A. | 鉴别乙烷与乙烯或除去乙烷中的少量乙烯杂质都可用高锰酸钾酸性溶液 | |
| B. | 某同学需用480 mL 2.0 moI•L-1氢氧化钠溶液进行实验,则配制该溶液时他称取氢氧化钠固体质量一定是38.4 g | |
| C. | 向含Fe3+的溶液中加入KSCN溶液时一定有红褐色沉淀产生 | |
| D. | 硝酸钾和稀硫酸的混合溶液中加入铜粉后,溶液会慢慢变蓝 |
6.把3mL NO2气体依次通过下列3个分别装有足量的①饱和NaHCO3溶液,②浓硫酸,③Na2O2固体的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内的气体应是( )
| A. | 1 mL NO | B. | 2 mL NO2和0.5 mL O2 | ||
| C. | 2 mL O2 | D. | 0.25 mL O2 |
3.下列离子能大量共存,且满足相应条件的是( )
| 选项 | 离子组 | 条件 |
| A | K+、Na+、Cu2+、Cl- | 溶液呈无色 |
| B | Na+、Fe3+、NO3-、SO42- | 滴入酸性KMnO4溶液,溶液褪色 |
| C | Al3+、SO42-、Cl-、H+ | 加入氨水产生白色沉淀后沉淀溶解 |
| D | Na+、NO3-、I-、SO42- | 加入盐酸和淀粉溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关化学用语表示正确的是( )
| A. | 用电子式表示HCl的形成过程: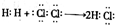 | |
| B. | Mg2+的结构示意图: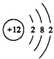 | |
| C. | HClO的结构式:H-Cl-O | |
| D. | 质量数为133,中子数为78的铯原子:${\;}_{55}^{133}$Cs |
1.化学与生产,生活息息相关,下叙述错误的是( )
| A. | 大量化石燃料的燃烧是造成雾霾天气的一种重要因素 | |
| B. | 含重金属离子的电镀液不能随意排放 | |
| C. | 煤经过汽化和液化两个物理变化过程后变为清洁能源,这是煤的综合利用的方法 | |
| D. | 改进汽车尾气净化技术,减少大气污染物的排放 |
20.下列实验操作正确的是( )
0 173455 173463 173469 173473 173479 173481 173485 173491 173493 173499 173505 173509 173511 173515 173521 173523 173529 173533 173535 173539 173541 173545 173547 173549 173550 173551 173553 173554 173555 173557 173559 173563 173565 173569 173571 173575 173581 173583 173589 173593 173595 173599 173605 173611 173613 173619 173623 173625 173631 173635 173641 173649 203614
| A. |  闻气体气味 | B. |  加热水 | C. |  倾倒液体 | D. |  移走蒸发皿 |
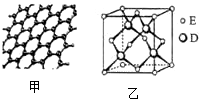 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: