13.下列说法正确的是( )
| A. | 棉花和蚕丝的主要成分都是纤维素 | |
| B. | 蛋白质在一定条件发生水解反应生成葡萄糖 | |
| C. | 煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程 | |
| D. | 食用植物油的主要成分是不饱和高级脂肪酸甘油酯,属于高分子化合物 |
12.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ba2+、Fe3+、CO32-、SO42-,现每次取100.00ml进行实验.
①第一份加入AgNO3溶液有沉淀产生.
②第二份加足量NaOH后加热,收集到气体0.896L(标准状态下).
③第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩2.33g.
试回答有关问题:
(1)通过实验①、②、③和必要计算,填写下表中部分离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?).
(2)判断K+是,最小浓度为0.2mol•L-1(填是或否)存在,若存在,求出其最小浓度,若不存在说明理由:-.
①第一份加入AgNO3溶液有沉淀产生.
②第二份加足量NaOH后加热,收集到气体0.896L(标准状态下).
③第三份加足量BaCl2后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩2.33g.
试回答有关问题:
(1)通过实验①、②、③和必要计算,填写下表中部分离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?).
| 部分离子 | Cl- | CO32- | SO42- | NH4+ | Ba2+ |
| c/(mol•L-1) | 无法确定 | 0.2 | 0.1 | 0.4 | 0 |
11.用于青奥村工程的隔热保温材料聚氨酯属于( )(填字母).
| A. | 有机高分子材料 | B. | 无机非金属材料 | C. | 金属材料 |
8.常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为kJ•mol-1)请根据下表一些键能数据完成下列问题.
(1)由表中数据规律预测C-Br键的键能范围:218 kJ•mol-1<C-Br键能<330 kJ•mol-1(填写数值和单位).
(2)已知下列热化学方程式:
O2(g)═O2+(g)+e-△H1=+1 175.7kJ/mol
PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ/mol
O2+PtF6-(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ/mol
则反应O2(g)+PtF6(g)═O2+PtF6-(s)△H=-77.6kJ•mol-1.
| 化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
| C-F | 427 | C-Cl | 330 | C-I | 218 |
| H-H | 436 | S=S | 255 | H-S | 339 |
(2)已知下列热化学方程式:
O2(g)═O2+(g)+e-△H1=+1 175.7kJ/mol
PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ/mol
O2+PtF6-(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ/mol
则反应O2(g)+PtF6(g)═O2+PtF6-(s)△H=-77.6kJ•mol-1.
7.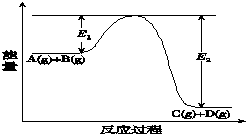 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
①图中E1代表的意义是反应物的活化能.
该反应是放热反应(填“吸热”或“放热”).反应热△H的表达式为E1-E2 .
②当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”).
(2)800℃时,在2L密闭容器内充入0.50mol NO和0.25mol O2,发生如下反应:2NO(g)+O2(g)═2NO2(g)△H<0.体系中,n(NO)随时间的变化如下表:
①能说明该反应已达到平衡状态的是BCD.
A.v(NO2)正=v(O2)逆 B.容器内压强保持不变
C.v(NO)逆=2v(O2)正D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是BC.
A.适当升高温度 B.缩小反应容器的体积C.增大O2的浓度 D.选择高效催化剂.
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题.①图中E1代表的意义是反应物的活化能.
该反应是放热反应(填“吸热”或“放热”).反应热△H的表达式为E1-E2 .
②当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”).
(2)800℃时,在2L密闭容器内充入0.50mol NO和0.25mol O2,发生如下反应:2NO(g)+O2(g)═2NO2(g)△H<0.体系中,n(NO)随时间的变化如下表:
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.50 | 0.35 | 0.28 | 0.25 | 0.25 | 0.25 |
A.v(NO2)正=v(O2)逆 B.容器内压强保持不变
C.v(NO)逆=2v(O2)正D.容器内气体颜色不变
②能使该反应的反应速率增大,且平衡向正反应方向移动的措施是BC.
A.适当升高温度 B.缩小反应容器的体积C.增大O2的浓度 D.选择高效催化剂.
6.某无色透明溶液能与铝粉反应放出H2,则此溶液中可能存在( )
| A. | OH-、Ba2+、Cl-、Na+ | B. | H+、Cl-、Na+、SO${\;}_{4}^{2-}$ | ||
| C. | H+、Cu2+、[Al(OH)4]-、SO${\;}_{4}^{2-}$ | D. | H+、Ba2+、Mg2+、NO${\;}_{3}^{-}$ |
5.下列反应的离子方程式正确的是( )
0 173433 173441 173447 173451 173457 173459 173463 173469 173471 173477 173483 173487 173489 173493 173499 173501 173507 173511 173513 173517 173519 173523 173525 173527 173528 173529 173531 173532 173533 173535 173537 173541 173543 173547 173549 173553 173559 173561 173567 173571 173573 173577 173583 173589 173591 173597 173601 173603 173609 173613 173619 173627 203614
| A. | 碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 25mL 0.3mol•L-1的FeBr2溶液中通入224mL标准状况下的氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| C. | 100mL 0.1mol•L-1的Al2(SO4)3溶液中加入20mL 3.5mol•L-1的NaOH溶液:Al3++4OH-═[Al(OH)4]- | |
| D. | 过量铁粉和稀硝酸反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |