6.分离汽油和水的混合溶液可选用的最好的方法是( )
| A. | 过滤 | B. | 蒸发 | C. | 分液 | D. | 萃取 |
5.证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是 ( )
| A. | 测定溶液的pH | B. | 加入Ba(OH)2溶液 | ||
| C. | 加入盐酸 | D. | 加入品红溶液 | ||
| E. | 用蓝色石蕊试纸检测 |
4.25℃,两种酸的电离平衡常数如下表.[已知:Ksp(MnS)=2.8×10-13]
①0.10mol•L-1Na2SO3溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为H2SO3+HCO3-=HSO3-+CO2↑+H2O.
1..下列有关化学用语表示正确的是( )
| A. | CH4分子的球棍模型: | |
| B. | 中子数为146、质子数为92的铀原子${\;}_{92}^{146}$U | |
| C. | 氟化钠的电子式: | |
| D. | 正丁烷的结构简式:C4H10 |
20.下列说法正确的是( )
| A. | 仅含有碳和氢两种元素的有机物称为烃 | |
| B. | 凡是分子里含碳元素的化合物都属于有机物 | |
| C. | 甲烷可以使酸性高锰酸钾溶液褪色 | |
| D. | 甲烷与氯气混合光照一段时间后黄绿色变浅,因为发生了置换反应 |
19.化学与人类生活密切相关,下列与化学有关的说法不正确的是( )
| A. | 化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 含氟牙膏可以有效防止龋齿 | |
| D. | 化学药品着火,都要立即用水或泡沫灭火器灭火 |
18.25℃时,两种酸的电离平衡常数如表:
(1)HSO${\;}_{3}^{-}$的电离平衡常数表达式K=$\frac{c(S{{O}_{3}}^{2-})•c({H}^{+})}{c(HS{{O}_{3}}^{-})}$
(2)请根据两种酸的电离平衡常数比较酸陛:H2SO3大于(大于、小于或等于)H2CO3.某同学设计实验比较两者的酸性:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量两溶液的c(H十).该实验设计不正确,错误在于用于比较pH的两种溶液的物质的量浓度不相等
(3)请用Na2CO3,H2SO4两种溶液,设计方案证明H2SO3和H2CO3的酸性强弱.
操作方法:向盛有亚硫酸溶液的试管中滴加碳酸钠溶液
实验现象:试管中有无色无味的气体产生.
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
(2)请根据两种酸的电离平衡常数比较酸陛:H2SO3大于(大于、小于或等于)H2CO3.某同学设计实验比较两者的酸性:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量两溶液的c(H十).该实验设计不正确,错误在于用于比较pH的两种溶液的物质的量浓度不相等
(3)请用Na2CO3,H2SO4两种溶液,设计方案证明H2SO3和H2CO3的酸性强弱.
操作方法:向盛有亚硫酸溶液的试管中滴加碳酸钠溶液
实验现象:试管中有无色无味的气体产生.
17.用水稀释0.1mol/L一元弱酸HX时,溶液中随着水量的增加而增大的是( )
0 173421 173429 173435 173439 173445 173447 173451 173457 173459 173465 173471 173475 173477 173481 173487 173489 173495 173499 173501 173505 173507 173511 173513 173515 173516 173517 173519 173520 173521 173523 173525 173529 173531 173535 173537 173541 173547 173549 173555 173559 173561 173565 173571 173577 173579 173585 173589 173591 173597 173601 173607 173615 203614
| A. | c(H+) | B. | c(X-) | C. | $\frac{c({H}^{+})}{c(HX)}$ | D. | $\frac{c(HX)}{c({H}^{+})}$ |
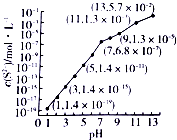 研究硫元素及其化合物的性质具有重要意义.
研究硫元素及其化合物的性质具有重要意义.