16.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O,
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
13.用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硫酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性:MnO2>Cl2>Br2 | |
| C | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
11.遇有下列情况,处理不当的是( )
| A. | 不小心将少量浓硫酸沾到皮肤上,立即用水冲洗 | |
| B. | 皮肤上沾有苯酚时,立即用酒精擦洗 | |
| C. | 误食重金属盐,立即喝生牛奶或蛋清 | |
| D. | 金属钠着火,立刻用砂子盖灭 |
8.下列说法不正确的是( )
| A. | 含铅汽油、含磷洗涤剂的使用均可对环境造成危害 | |
| B. | 棉花、木材及草类的纤维都是天然纤维 | |
| C. | 氮化硅陶瓷、光导纤维均属于新型无机非金属材料 | |
| D. | 煤、石油、天然气均属于可再生的化石燃料 |
7.为了测定一置于空气中的某硫酸酸化的FeSO4溶液中Fe2+被氧化的程度,某同学准确量取pH=1(忽略Fe2+、Fe3+的水解)的FeSO4溶液200mL,加入过量的BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀27.96g;再另取同样的FeSO4溶液200mL,向其中加入过量的NaOH溶液,搅拌使其充分反应,待沉淀全部变为红褐色后,过滤、洗涤并灼烧所得固体,最终得到固体的质量为8.00g
(1)计算该溶液中各种离子的浓度,并相应的填入下表:
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量浓度
(2)原溶液中Fe2+被氧化的百分率(被氧化的Fe2+物质的量占Fe2+和Fe3+总物质的量的百分比)20%.
(3)当Fe2+部分被氧化时,推导c(Fe2+、Fe3+)与c(H+)、c(SO42-)的关系是c(SO42-)-$\frac{1}{2}$c(H+)>c(Fe2+、Fe3+)>$\frac{2}{3}$c(SO42-)-$\frac{1}{3}$c(H+).
0 173416 173424 173430 173434 173440 173442 173446 173452 173454 173460 173466 173470 173472 173476 173482 173484 173490 173494 173496 173500 173502 173506 173508 173510 173511 173512 173514 173515 173516 173518 173520 173524 173526 173530 173532 173536 173542 173544 173550 173554 173556 173560 173566 173572 173574 173580 173584 173586 173592 173596 173602 173610 203614
(1)计算该溶液中各种离子的浓度,并相应的填入下表:
| c (H+) | c(SO42-) | c (Fe2+、Fe3+) |
(2)原溶液中Fe2+被氧化的百分率(被氧化的Fe2+物质的量占Fe2+和Fe3+总物质的量的百分比)20%.
(3)当Fe2+部分被氧化时,推导c(Fe2+、Fe3+)与c(H+)、c(SO42-)的关系是c(SO42-)-$\frac{1}{2}$c(H+)>c(Fe2+、Fe3+)>$\frac{2}{3}$c(SO42-)-$\frac{1}{3}$c(H+).
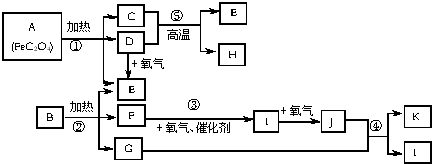
 元素及其化合物在生产、生活中有广泛应用.请回答下列问题:
元素及其化合物在生产、生活中有广泛应用.请回答下列问题: .
. .
.
 ;
;