6.下列关于σ键和π键说法正确的是( )
| A. | σ键是由两个p电子“肩并肩”重叠形成的 | |
| B. | σ键和π键都是共价键,σ键比π键更稳定 | |
| C. | 乙烯分子中的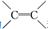 和乙炔分子中的-C≡C-都是π键 和乙炔分子中的-C≡C-都是π键 | |
| D. | H2分子中含有σ键,HCl分子中含π键 |
5.现有下列短周期元素性质的有关数据:
(1)根据元素周期律确定a至h 8种元素在周期表中的位置,将它们的元素编号填入下表相应的空格内.
(2)上述元素形成的氢化物中,分子间存在氢键的有(填氢化物的化学式)HF、NH3.
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛.在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH).
①氢化铝锂易水解,最初得三种产物,请写出其水解反应方程式LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑.
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请写出这种还原剂的电子式.写出该物质受热分解的反应方程式:2NaBH4$\frac{\underline{\;\;△\;\;}}{\;}$2B+2NaH+3H2↑.
(4)原子数相同,电子总数相同的分子或离子互称等电子体.在元素周期表中,与碳相邻的两种元素可形成具有石墨型晶体结构的“白石墨”,“白石墨”和石墨具有等电子体特征,写出“白石墨”的最小结构单元-六元环的结构式 .
.
| 元素符号 | a | b | c | d | e | f | g | h |
| 原子半径/mm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合计 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
| 族/周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | ||||||||
| 3 |
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛.在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH).
①氢化铝锂易水解,最初得三种产物,请写出其水解反应方程式LiAlH4+4H2O=LiOH+Al(OH)3+4H2↑.
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请写出这种还原剂的电子式.写出该物质受热分解的反应方程式:2NaBH4$\frac{\underline{\;\;△\;\;}}{\;}$2B+2NaH+3H2↑.
(4)原子数相同,电子总数相同的分子或离子互称等电子体.在元素周期表中,与碳相邻的两种元素可形成具有石墨型晶体结构的“白石墨”,“白石墨”和石墨具有等电子体特征,写出“白石墨”的最小结构单元-六元环的结构式
 .
.
4.下列离子方程式中正确的是( )
| A. | FeO溶于稀硝酸中:FeO+2H+=Fe2++H2O | |
| B. | 过量氨水加入AlCl3溶液中:Al3++3OH-=Al(OH)3↓ | |
| C. | 金属钠溶于水中:Na+H2O=Na++OH-+H2↑ | |
| D. | 过量CO2通入NaOH溶液中:OH-+CO2=HCO3- |
3. 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )| A. | 铁钉表面发生的反应为Fe-3e-=Fe3+ | |
| B. | 若液体a为稀盐酸,则U形管液面右高左低 | |
| C. | 若液体a为食盐水,则U形管液面左高右低 | |
| D. | 若液体a为食用油,则铁钉生锈速率较慢 |
2.下列叙述正确的是( )
| A. | Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 | |
| B. | 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铜 | |
| C. | 将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 | |
| D. | 过量的铜与浓硝酸反应,生成的气体只有NO2 |
19.下列说法中正确的是( )
| A. | 在水电离出的c(H+)=1×10-13mol/L的溶液中下列离子一定能大量共存:Na+、CO32-、Cl-、K+ | |
| B. | 氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同 | |
| C. | K2SO3溶液中c(K+)与c(SO32-)之比为2:1 | |
| D. | 硫酸是强电解质,故纯硫酸能导电 |
18.氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
(1)根据如图1能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
①该反应的平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$
②试判断K1>K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
④在某一时间段中反应速率与反应过程的曲线关系如图2,则图中氨的百分含量最低的时间段是D
A.t0-t1 B.t2-t3 C.t3-t4 D.t5-t6
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示,下列说法正确的是CD.
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C
d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.075mol/(L.min).

(1)根据如图1能量变化示意图,请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1>K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是c(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
④在某一时间段中反应速率与反应过程的曲线关系如图2,则图中氨的百分含量最低的时间段是D
A.t0-t1 B.t2-t3 C.t3-t4 D.t5-t6
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图3所示,下列说法正确的是CD.
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C
d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.075mol/(L.min).

17.下列说法错误的是( )
0 173409 173417 173423 173427 173433 173435 173439 173445 173447 173453 173459 173463 173465 173469 173475 173477 173483 173487 173489 173493 173495 173499 173501 173503 173504 173505 173507 173508 173509 173511 173513 173517 173519 173523 173525 173529 173535 173537 173543 173547 173549 173553 173559 173565 173567 173573 173577 173579 173585 173589 173595 173603 203614
| A. | 硅胶可用作食品干操剂 | |
| B. | P2O5不可用作食品干操剂 | |
| C. | 六水氯化钙可用作食品干燥剂 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
 物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是:
物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是: