10.下列物质属于碱的是( )
| A. | CaO | B. | C2H5OH | C. | Na2CO3 | D. | KOH |
7.半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)

已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3.PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中所装试剂是浓H2SO4,F中碱石灰的作用是吸收多余的氯气,防止空气中的水汽进入烧瓶与PC13反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后.通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.

已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3.PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中所装试剂是浓H2SO4,F中碱石灰的作用是吸收多余的氯气,防止空气中的水汽进入烧瓶与PC13反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后.通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
4.下列离子方程式正确的是( )
| A. | 碳酸钙溶于盐酸中:CO32-+2H+=H2O+CO2↑ | |
| B. | 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O | |
| D. | 用氢氧化钠溶液吸收少量二氧化碳:2OH-+CO2=CO32-+H2O |
3.下列实验操作正确的是( )
0 173040 173048 173054 173058 173064 173066 173070 173076 173078 173084 173090 173094 173096 173100 173106 173108 173114 173118 173120 173124 173126 173130 173132 173134 173135 173136 173138 173139 173140 173142 173144 173148 173150 173154 173156 173160 173166 173168 173174 173178 173180 173184 173190 173196 173198 173204 173208 173210 173216 173220 173226 173234 203614
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,冷凝水应从冷凝管上口进,下口出 | |
| C. | 过滤时,用玻璃棒搅拌以加速过滤 | |
| D. | 用酒精萃取碘水中的碘 |

 +
+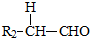 $→_{△}^{稀NaOH}$
$→_{△}^{稀NaOH}$ (R,R’为烃基或氢)
(R,R’为烃基或氢)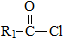 +R2OH$\stackrel{一定条件}{→}$
+R2OH$\stackrel{一定条件}{→}$ +HCl (R,R’为烃基)
+HCl (R,R’为烃基) .
.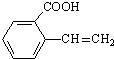 、
、 、
、 、
、 (其中之一).
(其中之一). .
.
 .
.