5. 乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下:
乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下: +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$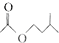 +H2O
+H2O
实验步骤:
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.回答下列问题:

(1)装置B的名称是:球形冷凝管
(2)在洗涤操作中,第一次水洗的主要目的是:洗掉大部分硫酸和醋酸; 第二次水洗的主要目的是:洗掉碳酸氢钠
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后D(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:提高醇的转化率
(5)实验中加入少量无水硫酸镁的目的是:干燥乙酸异戊酯;
(6)在蒸馏操作中,如图2仪器选择及安装都正确的是:b(填标号)
(7)本实验的产率是:C
A.30% B.40% C.50% D.60%
(8)在进行蒸馏操作时,若从130℃开始收集馏分,产率偏高(填高或者低)原因是会收集少量的未反应的异戊醇.
 乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下:
乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下: +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O| 相对分子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙醇 | 60 | 1.0492 | 118 | 溶 |
| 乙醇异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g的异戊醇,6.0g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.回答下列问题:

(1)装置B的名称是:球形冷凝管
(2)在洗涤操作中,第一次水洗的主要目的是:洗掉大部分硫酸和醋酸; 第二次水洗的主要目的是:洗掉碳酸氢钠
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后D(填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:提高醇的转化率
(5)实验中加入少量无水硫酸镁的目的是:干燥乙酸异戊酯;
(6)在蒸馏操作中,如图2仪器选择及安装都正确的是:b(填标号)
(7)本实验的产率是:C
A.30% B.40% C.50% D.60%
(8)在进行蒸馏操作时,若从130℃开始收集馏分,产率偏高(填高或者低)原因是会收集少量的未反应的异戊醇.
1.某同学设计实验制备2-羟基-4-苯基丁酸乙酯,反应原理、装置和数据如下:
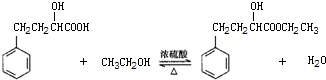
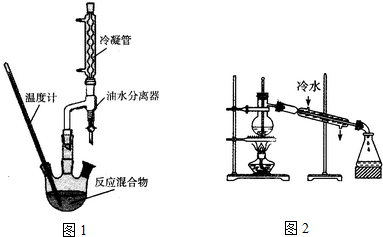
实验步骤:
①如图1,在干燥的圆底烧瓶中加入20mL 2-羟基-4-苯基丁酸、20mL无水乙醇和适量浓硫酸,再加入几粒沸石;
②加热至70℃左右保持恒温半小时;
③分离、提纯三颈瓶中的粗产品,得到有机粗产品;
④精制产品.
请回答下列问题:
(1)油水分离器的作用为及时分离产物水,促进平衡向生成酯的反应方向移动
(2)本实验采用水浴加热,因为温度过高会使产率减小(填“增大”、“”减小”或“不变”)
(3)取三颈烧瓶中的混合物分别用水、饱和碳酸氢钠溶液和水洗涤.第二次水洗的目的是洗掉碳酸氢钠
(4)在精制产品时,加入无水MgSO4的作用为干燥;然后过滤,再利用如图2装置进行蒸馏纯化,图2装置中的错误有温度计水银球的位置,冷凝水的方向
(5)若按纠正后的操作进行蒸馏纯化,并收集212℃的馏分,得2-羟基-4-苯基丁酸乙酯约9.0g.则该实验的产率为32%.


| 相对分子量 | 密度(g/cm3) | 沸点(℃) | 水溶性 | |
| 2-羟基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
| 乙 醇 | 46 | 0.789 | 78.4 | 易溶 |
| 2-羟基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 难溶 |
①如图1,在干燥的圆底烧瓶中加入20mL 2-羟基-4-苯基丁酸、20mL无水乙醇和适量浓硫酸,再加入几粒沸石;
②加热至70℃左右保持恒温半小时;
③分离、提纯三颈瓶中的粗产品,得到有机粗产品;
④精制产品.
请回答下列问题:
(1)油水分离器的作用为及时分离产物水,促进平衡向生成酯的反应方向移动
(2)本实验采用水浴加热,因为温度过高会使产率减小(填“增大”、“”减小”或“不变”)
(3)取三颈烧瓶中的混合物分别用水、饱和碳酸氢钠溶液和水洗涤.第二次水洗的目的是洗掉碳酸氢钠
(4)在精制产品时,加入无水MgSO4的作用为干燥;然后过滤,再利用如图2装置进行蒸馏纯化,图2装置中的错误有温度计水银球的位置,冷凝水的方向
(5)若按纠正后的操作进行蒸馏纯化,并收集212℃的馏分,得2-羟基-4-苯基丁酸乙酯约9.0g.则该实验的产率为32%.
20.Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用.
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:3FeS2+8O2$\frac{\underline{\;高温\;}}{\;}$6SO2+Fe304有3mol FeS2参加反应,转移32mol电子.
(2)自来水厂常用高铁酸钠(Na2Fe04)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理FeO42-有强的氧化性,能杀菌消毒,本身被还原为Fe3+,Fe3+发生水解生成氢氧化铁胶体吸附水中的杂质,达到净水的目的
(3)氧化铁是重要工业颜料,工业上利用废铁屑(含少量氧化铝、氧化铁等)生产它的工艺流程如下:
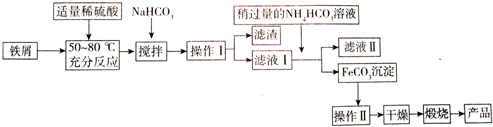
已知部分阳离子以氢氧化物形式沉淀的pH值见下表:
回答下列问题:
①操作I、Ⅱ的名称分别是过滤、洗涤
②铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,其目的是除去铁屑表面的油污
③铁屑与稀硫酸反应时,需加入过量铁屑的原因是(用离子反应方程式表示)Fe+2Fe3+=3Fe2+
④加入少量NaHCO3的目的是调节溶液pH,应控制pH的范围为4.4~7.5
⑤写出在空气中煅烧FeCO3的化学方程式4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2
⑥有些同学认为滤液Ⅰ中铁元素含量可用一定浓度的KMnO4溶液来测定,其设计的下列滴定方式中,最合理的是b.(夹持部分略去)(填字母序号)

(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:3FeS2+8O2$\frac{\underline{\;高温\;}}{\;}$6SO2+Fe304有3mol FeS2参加反应,转移32mol电子.
(2)自来水厂常用高铁酸钠(Na2Fe04)改善水质.简述高铁酸钠用于杀菌消毒同时又起到净水作用的原理FeO42-有强的氧化性,能杀菌消毒,本身被还原为Fe3+,Fe3+发生水解生成氢氧化铁胶体吸附水中的杂质,达到净水的目的
(3)氧化铁是重要工业颜料,工业上利用废铁屑(含少量氧化铝、氧化铁等)生产它的工艺流程如下:

已知部分阳离子以氢氧化物形式沉淀的pH值见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 沉淀完全 | 3.2 | 9.7 | 4.4 |
①操作I、Ⅱ的名称分别是过滤、洗涤
②铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,其目的是除去铁屑表面的油污
③铁屑与稀硫酸反应时,需加入过量铁屑的原因是(用离子反应方程式表示)Fe+2Fe3+=3Fe2+
④加入少量NaHCO3的目的是调节溶液pH,应控制pH的范围为4.4~7.5
⑤写出在空气中煅烧FeCO3的化学方程式4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2
⑥有些同学认为滤液Ⅰ中铁元素含量可用一定浓度的KMnO4溶液来测定,其设计的下列滴定方式中,最合理的是b.(夹持部分略去)(填字母序号)

18.肉桂酸是香料、化妆品、医药、浆料和感光树脂等的重要原料.实验室用如图1反应制取肉桂酸.

药品物理常数
填空:
I.合成:反应装置如图2所示.向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀.在150~170℃加热l小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)为了使温度便于控制,且受热均匀,该装置应采用的加热方法是空气浴(或油浴).加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
(3)不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解.
Ⅱ.粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
[反应混合物]$→_{硫酸钠溶液}^{加入饱和}$ $→_{苯甲醛}^{蒸馏除去}$ $\stackrel{盐酸酸化}{→}$ $\stackrel{操作1}{→}$ $→_{干燥}^{过滤、洗涤}$[肉桂酸品体】
(4)加饱和Na2CO3溶液除了转化醋酸,还有一个目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是冷却结晶;
(6)设计实验方案检验产品中是否含有苯甲醛取样,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛,或加入用新制氢氧化铜悬浊液,若出现砖红色沉淀,说明含有苯甲醛.
(7)若最后得到纯净的肉桂酸5.0g.则该反应中的产率是75%(保留两位有效数字).
0 172611 172619 172625 172629 172635 172637 172641 172647 172649 172655 172661 172665 172667 172671 172677 172679 172685 172689 172691 172695 172697 172701 172703 172705 172706 172707 172709 172710 172711 172713 172715 172719 172721 172725 172727 172731 172737 172739 172745 172749 172751 172755 172761 172767 172769 172775 172779 172781 172787 172791 172797 172805 203614

药品物理常数
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
| 相对分子质量 | 106 | 102 | 148 | 60 |
I.合成:反应装置如图2所示.向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀.在150~170℃加热l小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)为了使温度便于控制,且受热均匀,该装置应采用的加热方法是空气浴(或油浴).加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
(3)不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解.
Ⅱ.粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
[反应混合物]$→_{硫酸钠溶液}^{加入饱和}$ $→_{苯甲醛}^{蒸馏除去}$ $\stackrel{盐酸酸化}{→}$ $\stackrel{操作1}{→}$ $→_{干燥}^{过滤、洗涤}$[肉桂酸品体】
(4)加饱和Na2CO3溶液除了转化醋酸,还有一个目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是冷却结晶;
(6)设计实验方案检验产品中是否含有苯甲醛取样,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛,或加入用新制氢氧化铜悬浊液,若出现砖红色沉淀,说明含有苯甲醛.
(7)若最后得到纯净的肉桂酸5.0g.则该反应中的产率是75%(保留两位有效数字).
 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色