15.下列指定反应的离子方程式正确的是( )
| A. | SO2通入过量的氨水中:SO2+NH3•H2O═NH4++HSO3- | |
| B. | FeO溶于过量稀硝酸中:FeO+2H+═Fe2++H2O | |
| C. | NH4Al(SO4)2溶液中加入过量NaOH溶液中:NH4++Al3++4OH-═NH3•H2O+Al(OH)3↓ | |
| D. | 铜溶于酸化的H2O2溶液中:Cu+H2O2+2H+═Cu2++2H2O |
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol Cl2参加反应,转移的电子数目一定为0.2NA | |
| B. | 1.4g聚乙烯中含C-H数目为0.2NA | |
| C. | 标准状况下,5.6L甲醇中含有的分子数目为0.2NA | |
| D. | 常温下,pH=13的NaOH溶液中含OH-的数目为0.1NAA |
13.铜和浓硫酸反应制取SO2气体并回收硫酸铜的实验,不能达到目的是( )

| A. | 用装置甲制取二氧化硫气体 | |
| B. | 用装置乙收集二氧化硫气体 | |
| C. | 用适量CuO粉末中和反应后溶液,用装置丙过滤 | |
| D. | 用装置丁蒸发浓缩CuSO4溶液 |
12.下列有关仪器的使用方法或实验操作不正确的是( )
| A. | 测定溶液pH时,pH试纸先用蒸馏水润湿 | |
| B. | 蒸馏实验中,蒸馏前必须在蒸馏烧瓶中加入碎瓷片 | |
| C. | 用盐酸滴定滴定氨水实验中,用甲基橙作指示剂以减小实验误差 | |
| D. |  用如图所示的方法排除碱式滴定管胶管中的气泡 用如图所示的方法排除碱式滴定管胶管中的气泡 |
11.下列关于化学用语的表示正确的是( )
| A. | 二氟化氧分子电子式: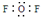 | |
| B. | 质子数与中子数相等的硫原子${\;}_{16}^{16}$S | |
| C. | 镁离子的结构示意图: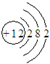 | |
| D. | 对甲基苯酚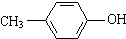 |
10.我省的海水资源丰富,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子.合理利用资源和保护环境是我省可持续发展的重要保证.
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据如表数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
(3)火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图1所示:

①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图2所示.请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据如表数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |

①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图2所示.请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
9.下列反应的离子方程式正确的是( )
| A. | 澄清石灰水中滴加少量的小苏打溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O | |
| C. | 过氧化钠和水反应:2O22-+2H2O═4OH-+O2↑ | |
| D. | H2O2溶液中滴加酸性KMnO4溶液:2MnO4-+5 H2O2+6H+═2Mn2++5O2↑+8H2O |
7.下列实验不能达到预期目的是( )
| A. | 用饱和食盐水除去Cl2中少量的HCl | |
| B. | 往溴水中通入SO2,可检验SO2的还原性和漂白性 | |
| C. | 往溶液加入盐酸,产生无色无味且能使澄清石灰水浑浊的气体,该气体一定是CO2 | |
| D. | 用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
6.下列因果关系叙述正确的是( )
0 172193 172201 172207 172211 172217 172219 172223 172229 172231 172237 172243 172247 172249 172253 172259 172261 172267 172271 172273 172277 172279 172283 172285 172287 172288 172289 172291 172292 172293 172295 172297 172301 172303 172307 172309 172313 172319 172321 172327 172331 172333 172337 172343 172349 172351 172357 172361 172363 172369 172373 172379 172387 203614
| A. | Fe3+有氧化性,实验室常用KSCN溶液检验Fe3+ | |
| B. | SO2有较强的还原性,SO2可使酸性KMnO4溶液褪色 | |
| C. | Mg有还原性,电解MgCl2饱和溶液可制备Mg | |
| D. | 浓H2SO4有吸水性,浓H2SO4可使蔗糖炭化 |
