8.一定温度下反应:A2(g)+3B2(g)?2AB3(g)(每生成2mol AB3放出92.4kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1mol A2和3mol B2,达平衡时放出热量为Q1,②通入2mol A2和6mol B2,达平衡时放出热量为Q2,则下列关系正确的是( )
| A. | Q2=2 Q1 | B. | 2Q1<Q2 | C. | Q1<Q2<92.4 kJ | D. | Q1=Q2<92.4 kJ |
5.历史上最早应用的还原性染料是靛蓝,其结构简式如图.下列关于靛蓝的叙述中错误的是( )

| A. | 该物质属于芳香族化合物 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 靛蓝完全燃烧生成二氧化碳和水 | D. | 它是不饱和的有机物 |
3.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y离子半径>Z离子半径(选填“>”、“=”、“<”).
(2)XY2是一种常用的溶剂,一个XY2的分子中存在2个σ键,2个π键.
(3)在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是F-S.
(4)向WYO4的水溶液中逐滴加入氨水至过量,观察到溶液由天蓝色最终变为深蓝色.反应过程中涉及的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
| 元素 | 相 关 信 息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | Y元素的激发态原子的电子排布式为1s22s22p63s23p34s1 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,一个XY2的分子中存在2个σ键,2个π键.
(3)在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是F-S.
(4)向WYO4的水溶液中逐滴加入氨水至过量,观察到溶液由天蓝色最终变为深蓝色.反应过程中涉及的离子方程式为:Cu2++2NH3•H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-.
2.“美丽中国”是十八大提出的重大课题,她突出了生态文明,重点是社会发展与自然环境之间的和谐,下列行为中不符合这一主题的是( )
| A. | 用已脱硫的煤作燃料 | |
| B. | 开发氢能等能源代替化石燃料,有利于保护环境 | |
| C. | 开发利用可燃冰是缓解能源紧缺的唯一途径 | |
| D. | 用“绿色化学”工艺,使原料尽可能转化为所需要的物质 |
1.离子检验的常用方法有三种:
下列离子检验的方法中不合理的是( )
| 验方法 | 沉淀法 | 显色法 | 气体法 |
| 判断的依据 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
| A. | CO32---气体法 | B. | SO42---沉淀法 | C. | H+--显色法 | D. | Cl---气体法 |
20.下列溶液中,与100mL 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 200 mL 0.25mol/L CaCl2溶液 | B. | 200 mL 0.25mol/L HCl溶液 | ||
| C. | 50 mL 1mol/L NaCl溶液 | D. | 100 mL 0.5mol/L MgCl2溶液 |
19.下列实验操作中,正确的是( )
0 172144 172152 172158 172162 172168 172170 172174 172180 172182 172188 172194 172198 172200 172204 172210 172212 172218 172222 172224 172228 172230 172234 172236 172238 172239 172240 172242 172243 172244 172246 172248 172252 172254 172258 172260 172264 172270 172272 172278 172282 172284 172288 172294 172300 172302 172308 172312 172314 172320 172324 172330 172338 203614
| A. | 向盛有10mL水的量筒中倒入浓硫酸即得稀硫酸 | |
| B. | 向试管中滴加试剂时,将滴管下端紧靠试管内壁 | |
| C. | 使用试纸检验溶液的性质时,将试纸浸入溶液中 | |
| D. | 用托盘天平称量药品时,左盘放药品,右盘放砝码 |
 如图为实验室制取蒸馏水的实验装置图:
如图为实验室制取蒸馏水的实验装置图:

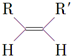 $\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO
$\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO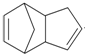 $\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$
$\stackrel{O_{3}}{→}$$\stackrel{H_{2}O/Zn}{→}$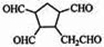 .
.