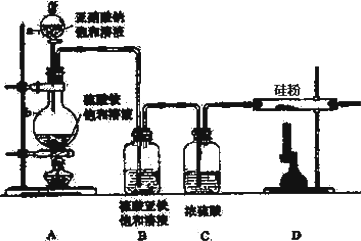
16.实验室制备间硝基苯胺的反应方程式、操作步骤、部分参考数据及装置图如图: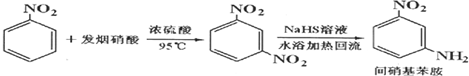
(发烟硝酸是溶有NO2的98%的浓硝酸)
①在圆底烧瓶中加入原料,加热搅拌使充分反应;
②将反应物倒入盛有碎冰的烧杯,待冷却结晶后倾倒出酸液,对剩余混合物进行抽滤;
③将滤出固体溶于甲醇,置于烧瓶中按照图1装置安装,并加入NaHS溶液,加热;
④反应充分后改为蒸馏装置(图2)蒸出溶剂,将残留液体倒入冷水,抽滤洗涤烘干.
已知:偶极矩可表示分子受固定相吸附的能力,越大吸附力越强请回答下列问题:

(1)步骤①中反应前期加热温度如超过95℃,易造成原料损失,故加热方式应为水浴加热;
(2)步骤②中抽滤的同时需用饱和Na2CO3溶液对固体进行洗涤,目的是洗去产物中混有的酸性物质,简述洗涤的操作过程在布氏漏斗中倒入饱和Na2CO3溶液至浸没固体后抽滤,重复若干次;
(3)步骤③装置(图1)中a仪器名称为干燥管,其中填充有碱石灰,作用是吸收挥发出的硝酸、NO2等酸性物质;
(4)关于步骤④装置(图2)相关叙述错误的是BCD;
A.冷凝水流向错误,应为低流进高流出
B.锥形瓶中首先收集到的液体为蒸馏水
C.温度计水银球位置偏低,应在液面以上,紧贴液面以迅速测定气体组分的温度
D.图1、2装置中b、c均有冷凝效果,故步骤④可在图1装置中直接完成蒸馏,无需改为图2装置
(5)最终得到的产品中含有少量邻硝基苯胺、对硝基苯胺以及硝基苯杂质,根据固定相对各组分在流动过程中的吸附能力大小可混合物分离.图3所示为混合物,已知C为间硝基苯胺,写出B的结构简式 ;
;
(6)之后该同学设计的提纯装置如图4:在一根底部带有旋塞的玻璃管内装满固定相,将流动相与样品混合后从上端倒入,并持续倒入流动相,一段时间后发现管内出现如图四段黄色色带,则本实验所需收集的产物组分主要集中在色带层② (填编号)上.

(发烟硝酸是溶有NO2的98%的浓硝酸)
①在圆底烧瓶中加入原料,加热搅拌使充分反应;
②将反应物倒入盛有碎冰的烧杯,待冷却结晶后倾倒出酸液,对剩余混合物进行抽滤;
③将滤出固体溶于甲醇,置于烧瓶中按照图1装置安装,并加入NaHS溶液,加热;
| 参考数据 | 组分 | 邻硝基苯胺 | 间硝基苯胺 | 对硝基苯胺 | 水 | 甲醇 | 硝基苯 |
| 沸点/℃ | 284 | 305.7 | 331.7 | 100 | 64.7 | 4.75 | |
| 偶极矩/D | 4.38 | 4.91 | 6.33 | 1.85 | 1.69 | 4.75 | |
| 颜色 | 橙色 | 淡黄色 | 淡黄色 | 无色 | 无色 | 淡黄色 |
已知:偶极矩可表示分子受固定相吸附的能力,越大吸附力越强请回答下列问题:

(1)步骤①中反应前期加热温度如超过95℃,易造成原料损失,故加热方式应为水浴加热;
(2)步骤②中抽滤的同时需用饱和Na2CO3溶液对固体进行洗涤,目的是洗去产物中混有的酸性物质,简述洗涤的操作过程在布氏漏斗中倒入饱和Na2CO3溶液至浸没固体后抽滤,重复若干次;
(3)步骤③装置(图1)中a仪器名称为干燥管,其中填充有碱石灰,作用是吸收挥发出的硝酸、NO2等酸性物质;
(4)关于步骤④装置(图2)相关叙述错误的是BCD;
A.冷凝水流向错误,应为低流进高流出
B.锥形瓶中首先收集到的液体为蒸馏水
C.温度计水银球位置偏低,应在液面以上,紧贴液面以迅速测定气体组分的温度
D.图1、2装置中b、c均有冷凝效果,故步骤④可在图1装置中直接完成蒸馏,无需改为图2装置
(5)最终得到的产品中含有少量邻硝基苯胺、对硝基苯胺以及硝基苯杂质,根据固定相对各组分在流动过程中的吸附能力大小可混合物分离.图3所示为混合物,已知C为间硝基苯胺,写出B的结构简式
 ;
;(6)之后该同学设计的提纯装置如图4:在一根底部带有旋塞的玻璃管内装满固定相,将流动相与样品混合后从上端倒入,并持续倒入流动相,一段时间后发现管内出现如图四段黄色色带,则本实验所需收集的产物组分主要集中在色带层② (填编号)上.
15.工业上可用焦炭与二氧化硅的混合物在高温下与氯气反应生成SiCl4和CO,SiCl4经提纯后用氢气还原得高纯硅.以下是实验室制备SiCl4的装置示意图.
已知:SiCl4熔点为-70.0℃,沸点为57.7℃,且遇水易水解.
(1)装置C中的试剂是浓硫酸:装置F的作用为防止F右端的水蒸气进入E与四氯化硅反应,造成产物不纯.
(2)装置A中发生反应的离子方程式为:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑.A装置中,有一处明显错误是无石棉网.
(3)装置D的硬质玻璃管中发生反应的化学方程式是SiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2CO.
(4)G中吸收气体一段时间后,吸收液中肯定存在OH-、Cl-和SO42-.为探究该吸收液中可能存在的其它酸根离子(忽略空气中CO2的影响).
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-:假设3:只有ClO-.
【设计方案,进行实验】可供选择的实验试剂有:3mol/L H2SO4溶液、1mol/L NaOH溶液、溴水、品红溶液、0.01mol/L KMnO4溶液、淀粉-KI溶液.
各取少量吸收液于a、b、c三支试管中,分别滴加适量的3mol/LH2SO4溶液后,进行下列实验.请完成下表:

已知:SiCl4熔点为-70.0℃,沸点为57.7℃,且遇水易水解.
(1)装置C中的试剂是浓硫酸:装置F的作用为防止F右端的水蒸气进入E与四氯化硅反应,造成产物不纯.
(2)装置A中发生反应的离子方程式为:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑.A装置中,有一处明显错误是无石棉网.
(3)装置D的硬质玻璃管中发生反应的化学方程式是SiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2CO.
(4)G中吸收气体一段时间后,吸收液中肯定存在OH-、Cl-和SO42-.为探究该吸收液中可能存在的其它酸根离子(忽略空气中CO2的影响).
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-:假设3:只有ClO-.
【设计方案,进行实验】可供选择的实验试剂有:3mol/L H2SO4溶液、1mol/L NaOH溶液、溴水、品红溶液、0.01mol/L KMnO4溶液、淀粉-KI溶液.
各取少量吸收液于a、b、c三支试管中,分别滴加适量的3mol/LH2SO4溶液后,进行下列实验.请完成下表:
| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4(或溴水)溶液 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红溶液 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 假设2成立 | ||
| ③ | 向C试管中滴加几滴淀粉-KI溶液 | 若溶液变为蓝色 | 假设3成立 |
13.某兴趣小组同学在实验室用加热1-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如图所示装置,其中夹持仪器、加热仪器及冷却水管没有画出.

请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管接通冷凝水,进水口是Ⅱ(填“I”或“Ⅱ”);冷凝回流的主要目的是充分反应,提高反应物的转化率.
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物.B、C中应盛放的试剂分别是石蕊试液(或AgNO3溶液)和溴水(或酸性KMnO4溶液),写出C装置中主要的化学方程式:CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 .
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
请你补充下列实验步骤,直到分离出1-溴丁烷.
①待烧瓶冷却后,拔去竖直的冷凝管;
②插上带橡皮塞的温度计;
③关闭a,打开b;
④接通冷凝管的冷凝水,使冷水从d处流入;
⑤迅速升高温度至101.6℃,收集所得馏分.
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,则1-溴丁烷的产率是70%.(保留2位有效数字)

请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷.竖直冷凝管接通冷凝水,进水口是Ⅱ(填“I”或“Ⅱ”);冷凝回流的主要目的是充分反应,提高反应物的转化率.
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等.熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物.B、C中应盛放的试剂分别是石蕊试液(或AgNO3溶液)和溴水(或酸性KMnO4溶液),写出C装置中主要的化学方程式:CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 .
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
①待烧瓶冷却后,拔去竖直的冷凝管;
②插上带橡皮塞的温度计;
③关闭a,打开b;
④接通冷凝管的冷凝水,使冷水从d处流入;
⑤迅速升高温度至101.6℃,收集所得馏分.
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g 1-溴丁烷,则1-溴丁烷的产率是70%.(保留2位有效数字)
11. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成Cu而使Cu2O产率降低.
(2)方法Ⅰ制备过程会产生有毒气体,每生成1g该有毒气体,能量变化a kJ,写出制备反应的热化学方程式2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+28akJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大,过滤(填操作名称)可分离出颗粒过大的Cu2O.
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;光照\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0水蒸气的浓度(mol•L-1)随时间t(min)变化如下表:
可以判断:实验①的前20 min的平均反应速率 ν(O2)=3.5×10-5 mol•L-1 min-1;实验温度T1<T2(填“>”、“<”);催化剂的催化效率:实验①<实验②(填“>”、“<”).
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:2Cu+H2O $\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(2)方法Ⅰ制备过程会产生有毒气体,每生成1g该有毒气体,能量变化a kJ,写出制备反应的热化学方程式2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+28akJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大,过滤(填操作名称)可分离出颗粒过大的Cu2O.
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g)$\frac{\underline{\;光照\;}}{Cu_{2}O}$2H2(g)+O2(g)△H>0水蒸气的浓度(mol•L-1)随时间t(min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
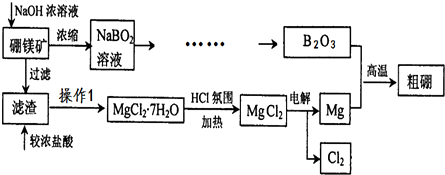
9.氮化硅的强度很高,尤其是热压氮化硅,是世界上最坚硬的物质之一,氮化硅陶瓷可做燃气轮机的燃烧室、机械密封环、输送铝液的电磁泵的管道及阀门、永久性模具、钢水分离环等.制备氮化硅可将硅粉放在氮气中加热至1000℃左右直接氮化制得,实验室制备氮化硅装置示意图如下:
回答下列问题:
(1)a仪器的名称是分液漏斗
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O
(3)装置B的作用是除去氧气(及氮氧化物),装置C的作用是除去水蒸气;
(4)已知氮化硅的化学性质稳定,但常温下易溶于氢氟酸溶液生成一种白色的胶状沉淀和一种盐,请写出此化学反应方程式:Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F;
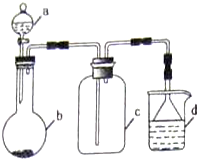
(5)实验室中某些气体的制取、收集及尾气处理装置如右图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D
0 171451 171459 171465 171469 171475 171477 171481 171487 171489 171495 171501 171505 171507 171511 171517 171519 171525 171529 171531 171535 171537 171541 171543 171545 171546 171547 171549 171550 171551 171553 171555 171559 171561 171565 171567 171571 171577 171579 171585 171589 171591 171595 171601 171607 171609 171615 171619 171621 171627 171631 171637 171645 203614

回答下列问题:
(1)a仪器的名称是分液漏斗
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O
(3)装置B的作用是除去氧气(及氮氧化物),装置C的作用是除去水蒸气;
(4)已知氮化硅的化学性质稳定,但常温下易溶于氢氟酸溶液生成一种白色的胶状沉淀和一种盐,请写出此化学反应方程式:Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F;
(5)实验室中某些气体的制取、收集及尾气处理装置如右图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是D

| 选项 | a物质 | b物质 | c收集的气体 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Fe | NO2 | H2O |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |