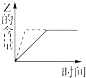
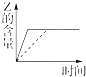
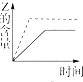
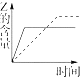
8.向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图1所示.图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.

已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c (B)未画出.
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=0.02mol•L-1•min-1.
(2)(2)t4-t5阶段改变的条件为减小压强,B的起始物质的量为1.0mol.各阶段平衡时对应的平衡常如表所示:
则K1=0.84(保留两位小数),K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5(用“>”“<”或“=”连接).
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g);△H=+200a kJ•mol-1.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4且b+$\frac{1}{3}$c=1.2.

已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c (B)未画出.
(1)若t1=15min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=0.02mol•L-1•min-1.
(2)(2)t4-t5阶段改变的条件为减小压强,B的起始物质的量为1.0mol.各阶段平衡时对应的平衡常如表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:2A(g)+B(g)?3C(g);△H=+200a kJ•mol-1.
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为a+$\frac{2}{3}$c=2.4且b+$\frac{1}{3}$c=1.2.
7. 在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
 在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )| A. | P3>P4,y轴表示A的物质的量 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均相对分子质量 |
6.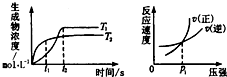 可逆反应aA(g)+bB(g)?cC(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )
 可逆反应aA(g)+bB(g)?cC(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )| A. | a+b>c+d T1<T2△H<0 | B. | a+b>c+d T1<T2△H>0 | ||
| C. | a+b<c+d T1>T2△H<0 | D. | a+b>c+d T1>T2△H>0 |
5. 密闭容器中反应:A2+B2?2AB,产物AB的生成情况如图所示,a为500℃,b为300℃时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是( )
密闭容器中反应:A2+B2?2AB,产物AB的生成情况如图所示,a为500℃,b为300℃时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是( )
 密闭容器中反应:A2+B2?2AB,产物AB的生成情况如图所示,a为500℃,b为300℃时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是( )
密闭容器中反应:A2+B2?2AB,产物AB的生成情况如图所示,a为500℃,b为300℃时的情况,c为300℃从时间t3开始向容器中加压的情况,下列叙述正确的是( )| A. | A2、B2、AB均为气体,正反应放热 | |
| B. | AB为气体,A2、B2中最少有一种为非气体,正反应吸热 | |
| C. | AB为气体,A2、B2中最少有一种为非气体,正反应放热 | |
| D. | AB为固体,A2、B2中最少有一种为非气体,正反应吸热 |
3.在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
请回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{C(CO{\;}_{2})•C(H{\;}_{2})}{C(CO)•C(H{\;}_{2}O)}$,该反应为放热反应(填“吸热”或
“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC.
A.容器中压强不变
B.混合气体中c(CO)不变
C.v生成(H2)=v消耗(H2)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,缩小容器的体积,平衡不移动(填“向正反应方向”、“向逆反应方向”或“不”).
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
| t/(℃) | 700 | 80 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的化学平衡常数表达式为K=$\frac{C(CO{\;}_{2})•C(H{\;}_{2})}{C(CO)•C(H{\;}_{2}O)}$,该反应为放热反应(填“吸热”或
“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC.
A.容器中压强不变
B.混合气体中c(CO)不变
C.v生成(H2)=v消耗(H2)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,缩小容器的体积,平衡不移动(填“向正反应方向”、“向逆反应方向”或“不”).
2. 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)?Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A. | 往平衡体系中加入少量金属铅后,c(Pb2+)增大 | |
| B. | 往平衡体系中加入少量 Sn(NO3)2固体后,c(Pb2+)变小 | |
| C. | 升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 | |
| D. | 25℃时,该反应的平衡常数K=2.2 |
20.在常温下,下列可逆反应的平衡移动伴随着颜色变化,但颜色变化不受压强变化影响的是( )
| A. | 2NO2?N2O4 | B. | 2NO2?2NO+O2 | ||
| C. | 2HI?H2+I2 | D. | FeCl3+3KSCN?Fe(SCN)3+3KCl |
19. 在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则下列叙述正确的是( )
在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则下列叙述正确的是( )
0 170442 170450 170456 170460 170466 170468 170472 170478 170480 170486 170492 170496 170498 170502 170508 170510 170516 170520 170522 170526 170528 170532 170534 170536 170537 170538 170540 170541 170542 170544 170546 170550 170552 170556 170558 170562 170568 170570 170576 170580 170582 170586 170592 170598 170600 170606 170610 170612 170618 170622 170628 170636 203614
 在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则下列叙述正确的是( )
在一定条件下,A气体与B气体反应生成C气体.反应过程中,反应物与生成物的浓度随时间变化的曲线如图,则下列叙述正确的是( )| A. | 该反应的化学方程式为3A+B?2C | |
| B. | 在t1~(t110)s时,v(A)=v(B)=0 | |
| C. | t1 s时反应物A转化率为60% | |
| D. | 0~t1 s内A的反应速率为v(A)=$\frac{0.2}{{t}_{1}}$mol/(L•s) |
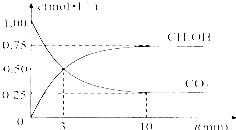 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.