14.下列关于有机物的说法错误的是( )
| A. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| B. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| C. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| D. | 石油和天然气的主要成分都是碳氢化合物 |
13.下列各组中的性质比较,正确的是( )
| A. | 酸性HClO4>HBrO4>HIO4 | B. | 碱性NaOH>Mg(OH)2>Ca(OH)2 | ||
| C. | 稳定性:HI>H2S>HCl | D. | 氧化性:Na+>Mg2+>Al3+ |
12.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| B. | 用惰性电极电解MgCl2溶液的反应原理:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- | |
| C. | 用惰性电极电解稀H2SO4溶液一段时间后,溶液的酸性增强 | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
9.用FeCl3酸性溶液脱除H2S后的溶液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol•L-1的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):
(1)用KSCN溶液检验出Fe3+的现象是溶液变红.
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应:2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-.
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
①NaCl溶液的浓度是0.2mol•L-1.
②Ⅳ中检测Cl2的实验方法取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出有关反应:2Cl--2e-=Cl2↑,Cl2+2Fe2+=2Fe3++2Cl-.
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检测Cl2的实验方法取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
8.设NA为阿伏加德罗常数,下列有关说法正确的是( )
0 170038 170046 170052 170056 170062 170064 170068 170074 170076 170082 170088 170092 170094 170098 170104 170106 170112 170116 170118 170122 170124 170128 170130 170132 170133 170134 170136 170137 170138 170140 170142 170146 170148 170152 170154 170158 170164 170166 170172 170176 170178 170182 170188 170194 170196 170202 170206 170208 170214 170218 170224 170232 203614
| A. | 常温下,2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| B. | 0.5 mol苯分子中含有C=C双键数为1.5 NA | |
| C. | 1 mol甲基(-CH3)所含的电子总数为10 NA | |
| D. | 标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为$\frac{{N}_{A}}{22.4}$ |
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.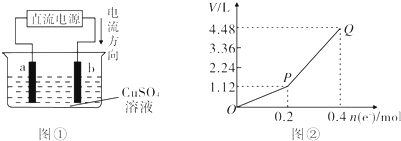
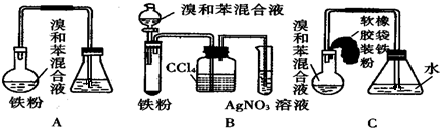
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$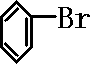 +HBr;装置A中左侧长导管的作用是导气和冷凝回流;装置A和C中的两处明显错误是锥形瓶未与大气相通、导管插入AgNO3(或水)溶液中.
+HBr;装置A中左侧长导管的作用是导气和冷凝回流;装置A和C中的两处明显错误是锥形瓶未与大气相通、导管插入AgNO3(或水)溶液中.
 利用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液,在如图所示装置中测定中和热,回答下列问题:
利用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液,在如图所示装置中测定中和热,回答下列问题: