16.下列指定的微粒的个数比为2:1的是( )
| A. | BaO2(过氧化钡)固体中的阳离子和阴离子 | |
| B. | ${\;}_{1}^{2}$H中的中子和质子 | |
| C. | NaHCO3中的阳离子和阴离子 | |
| D. | 4Be2+中的质子和电子 |
14.已知由石墨制备金刚石的反应为:C(石墨)$\frac{\underline{\;一定条件\;}}{\;}$C(金刚石);△H>0,则下列两个反应中:C(石墨)+O2(g)═CO2(g);△H=a kJ/mol,C(金刚石)+O2(g)═CO2(g);△H=b kJ/mol,a与b的关系为( )
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
13.在单质的晶体中,一定不存在( )
0 169980 169988 169994 169998 170004 170006 170010 170016 170018 170024 170030 170034 170036 170040 170046 170048 170054 170058 170060 170064 170066 170070 170072 170074 170075 170076 170078 170079 170080 170082 170084 170088 170090 170094 170096 170100 170106 170108 170114 170118 170120 170124 170130 170136 170138 170144 170148 170150 170156 170160 170166 170174 203614
| A. | 离子键 | B. | 分子间作用力 | C. | 共价键 | D. | 金属键 |
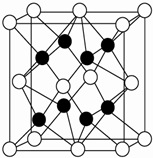 X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.
X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.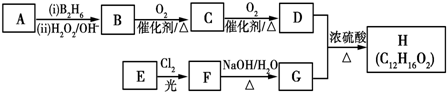
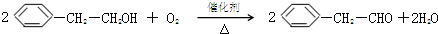 .
. .
.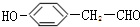 .
.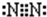 ;乙分子的结构式
;乙分子的结构式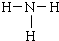 .
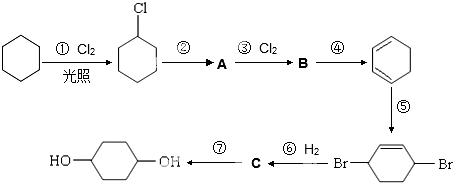
.
 ;
;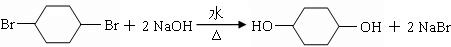 .
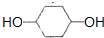
.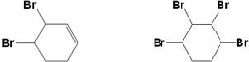 .
. +O2$→_{△}^{催化剂}$
+O2$→_{△}^{催化剂}$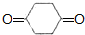 +2H2O.
+2H2O. +Br2→
+Br2→ ,反应类型为加成反应.
,反应类型为加成反应.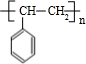 .
.