12.四种短周期元素在周期表中的位置如图,其中X元素的原子最外层电子数等于其电子层数.下列说法不正确的是( )
| Z | W | ||
| X | Y |
| A. | X元素最高价氧化物化学式为X2O3 | |
| B. | 原子半径:X>Y>Z>W | |
| C. | 最简单气态氢化物的热稳定性:W>Y | |
| D. | Y元素的最高价氧化物既能与NaOH溶液反应,也能与HF溶液反应,属于两性氧化物 |
11.表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是K,在③~⑦元素中,原子半径最大的是Mg;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式).
写出①和④的最高价氧化物对应的水化物反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
(3)用电子式表示③和⑨形成的化合物的形成过程 .
.
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式: ,该物质所含化学键类型离子键、共价键,0.1mol X与水反应转移电子数为:0.1NA
,该物质所含化学键类型离子键、共价键,0.1mol X与水反应转移电子数为:0.1NA
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式F-N=N-F.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 3 | ① | ③ | ④ | ⑨ | ||||
| 4 | ② |
(1)在上述元素中,金属性最强的是K,在③~⑦元素中,原子半径最大的是Mg;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式).
写出①和④的最高价氧化物对应的水化物反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O.
(3)用电子式表示③和⑨形成的化合物的形成过程
 .
.(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:
 ,该物质所含化学键类型离子键、共价键,0.1mol X与水反应转移电子数为:0.1NA
,该物质所含化学键类型离子键、共价键,0.1mol X与水反应转移电子数为:0.1NA(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式F-N=N-F.
8.在某温度下,将某NaOH溶液和0.1mol•L-1的HAc溶液充分混合后,则该混合溶液中有关离子的浓度应满足的关系是( )
| A. | [Na+]>[Ac-] | B. | [Na+]>[Ac-] | C. | [Na+]<[Ac-] | D. | [Na+]+[H+]=[OH-]+[Ac-] |
7.下列关于盐的水解的叙述中,正确的是( )
| A. | 盐类的水解过程是中和反应的逆过程,是吸热过程 | |
| B. | 易水解的盐溶于水后,都抑制了水的电离 | |
| C. | 易水解的盐溶液中,水电离出的以游离态存在的H+和OH-的浓度永远相等 | |
| D. | 易水解的盐溶液肯定不是中性的 |
6.下列物质在水溶液中存在着电离平衡的是( )
| A. | HF | B. | HNO3 | C. | C2H5OH(酒精) | D. | Na2SO4 |
5.等体积混合0.1mol•L-1的盐酸和0.06mol•L-1的Ba(OH )2溶液,不考虑体积效应,即认为混合溶液的体积等于进行混合的两溶液体积之和,溶液的pH值等于( )
0 169362 169370 169376 169380 169386 169388 169392 169398 169400 169406 169412 169416 169418 169422 169428 169430 169436 169440 169442 169446 169448 169452 169454 169456 169457 169458 169460 169461 169462 169464 169466 169470 169472 169476 169478 169482 169488 169490 169496 169500 169502 169506 169512 169518 169520 169526 169530 169532 169538 169542 169548 169556 203614
| A. | 2.0 | B. | 12.3 | C. | 1.7 | D. | 12.0 |
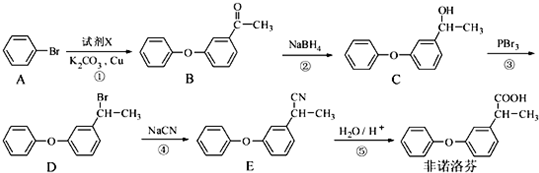
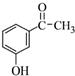 .
.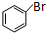 +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$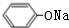 +NaBr+H2O.
+NaBr+H2O.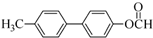 .
.