10.下列化学用语表示正确的是( )
| A. | HClO的电子式为: | |
| B. | 硝基苯的结构简式为: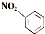 | |
| C. | 含18个中子的氯原子的核素符号:${\;}_{35}^{17}$Cl | |
| D. | 四氯化碳分子比例模型: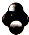 |
8.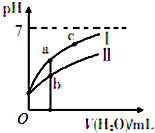 已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
(1)图象中,曲线Ⅰ表示的酸是CH3COOH(填化学式);起始时,c(CH3COOH)<c(HClO)
(填“>”、“<”、“=”).
(2)a、b、c三点中,水的电离程度由大到小的顺序是c>a>b(用编号表示).
(3)25℃时,NaClO溶液的水解平衡常数Kh=$\frac{1}{3}$×10-6mol•L-1.
(4)向NaClO溶液中通入少量CO2的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
 已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.
已知下表为25℃时某些弱酸的电离平衡常数;如图表示常温时,稀释CH3COOH、HC1O两种酸的稀溶液时,溶液pH随加水量的变化.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | K$_{{a}_{1}}$a1=4.4×10-7K$_{{a}_{2}}$a2=4.7×10-11 |
(填“>”、“<”、“=”).
(2)a、b、c三点中,水的电离程度由大到小的顺序是c>a>b(用编号表示).
(3)25℃时,NaClO溶液的水解平衡常数Kh=$\frac{1}{3}$×10-6mol•L-1.
(4)向NaClO溶液中通入少量CO2的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
7.在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

| A. | a点Kw=1.0×10-14 mol2•L-2 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:C(NH4+)>C(Cl-)>C(H+)>C(OH-) | |
| D. | 25℃时NH4Cl水解常数为(n-1)×10-7 mol•L-1(用n表示) |
6.在下列各溶液中,离子一定能大量共存的是( )
| A. | 碱性溶液中:K+、Mg2+、S2-、ClO- | |
| B. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、HCO3-、SO42- |
5.有机化合物M的结构简式为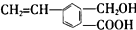 ,关于M的说法正确的是( )
,关于M的说法正确的是( )
 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | M中只有两种官能团 | |
| B. | 1 molM最多能消耗2 mol NaOH | |
| C. | M能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色 | |
| D. | M可以发生酯化、加成反应,不能发生聚合反应 |
4.食品安全、资源充分利用、保护环境备受关注,下列做法与此理念相违背的是( )
| A. | 食品中大量添加苯甲酸钠等防腐剂,可有效延长其保质期 | |
| B. | “地沟油”可以制成生物柴油,提高资源的利用率 | |
| C. | 发展光伏发电等高效清洁能源,缓解能源危机 | |
| D. | 大力发展公共交通,提高汽油的质量,对减轻雾霾很有必要 |
2.已知:
2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
H2(g)+0.5O2(g)=H2O(g)△H=-242kJ•mol-1
现有1mol液态水,蒸发时吸收的热量是( )
0 169276 169284 169290 169294 169300 169302 169306 169312 169314 169320 169326 169330 169332 169336 169342 169344 169350 169354 169356 169360 169362 169366 169368 169370 169371 169372 169374 169375 169376 169378 169380 169384 169386 169390 169392 169396 169402 169404 169410 169414 169416 169420 169426 169432 169434 169440 169444 169446 169452 169456 169462 169470 203614
2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
H2(g)+0.5O2(g)=H2O(g)△H=-242kJ•mol-1
现有1mol液态水,蒸发时吸收的热量是( )
| A. | 2.44 kJ | B. | 44 kJ | C. | 88 kJ | D. | 330 kJ |
 (1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充电}^{放电}$2PbSO4+2H2O.请回答下列问题(不考虑氢、氧的氧化还原):
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2$S{O}_{4}^{2-}$$?_{充电}^{放电}$2PbSO4+2H2O.请回答下列问题(不考虑氢、氧的氧化还原): 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答下列问题:
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答下列问题: