3.下列表示对应化学反应的离子方程式正确的是( )
| A. | 工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- | |
| B. | 碳酸钠的水解:CO32-+2H2O═H2CO3+2OH- | |
| C. | 硫酸铝溶液中滴加过量浓氨水:Al3++4 NH3•H2O═AlO${\;}_{2}^{-}$+4NH4++2H2O | |
| D. | 用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
2.在碱性条件下能够大量共存,而在强酸性条件下却能发生氧化还原反应的离子组是( )
| A. | Ba2+、AlO2-、NO3-、Cl- | B. | K+、Na+、ClO-、Fe2+ | ||
| C. | Na+、I-、NO3-、SO42- | D. | NH4+、Na+、S2-、CO32- |
19.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )


| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 原子半径:W>X>Y | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
18.下列叙述I和II均正确且具有因果关系的是( )
| 编号 | 叙述I | 叙述II |
| A | Fe3+的氧化性比Cu2+强 | FeCl3溶液可用于溶解回收旧电路板中的铜 |
| B | NH4Cl受热分解 | 加热可将Ca(OH)2和NH4Cl固体混合物分离 |
| C | 金属活动性铜比铁弱 | 镀铜铁制品表层划损后仍然受到保护 |
| D | Cl2具有漂白性 | 用氯气制盐酸 |
| A. | A | B. | B | C. | C | D. | D |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol苯中含有3nA个碳碳双键 | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
16.下列水溶液中能大量共存的一组离子是( )
| A. | K+、Al3+、CO32-、Cl- | B. | Na+、H+、SO42-、SiO32- | ||
| C. | H+、NH4+、SO42-、I- | D. | H+、Fe2+、Cl-、ClO- |
15.化学广泛应用于生活生产,下列说法正确的是( )
0 168356 168364 168370 168374 168380 168382 168386 168392 168394 168400 168406 168410 168412 168416 168422 168424 168430 168434 168436 168440 168442 168446 168448 168450 168451 168452 168454 168455 168456 168458 168460 168464 168466 168470 168472 168476 168482 168484 168490 168494 168496 168500 168506 168512 168514 168520 168524 168526 168532 168536 168542 168550 203614
| A. | 青铜器、硬币都属于纯净物 | |
| B. | 葡萄糖和银氨溶液发生银镜反应可用作制镜子 | |
| C. | 铺路用的沥青主要含有C、H、O等元素 | |
| D. | 鸡蛋清中加入胆矾可以使蛋白质发生盐析 |
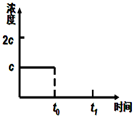 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题: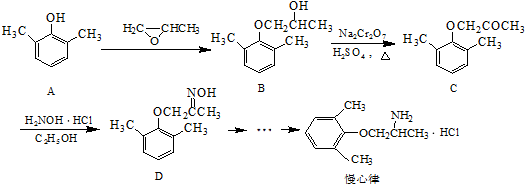
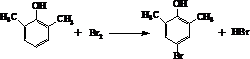 .
. .
.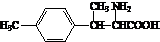 .
.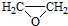 ).写出以邻甲基苯
).写出以邻甲基苯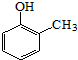 )和乙醇为原料制备
)和乙醇为原料制备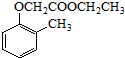 的合成路线流程图(无机试
的合成路线流程图(无机试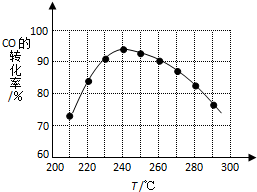 二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应: