9.下列反应的有机产物中,一定不存在同分异构体的反应是( )
| A. | 1,3-丁二烯(CH2=CH-CH=CH2)与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷( )与NaOH乙醇溶液共热发生消去HCl分子的反应 )与NaOH乙醇溶液共热发生消去HCl分子的反应 | |
| C. | 甲苯在一定条件下与足量硝酸发生硝化反应 | |
| D. | 乙醇与HBr发生的取代反应 |
8.由1,3丁二烯合成氯丁橡胶的过程中,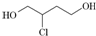 是一种中间产物.下列说法正确的是( )
是一种中间产物.下列说法正确的是( )
 是一种中间产物.下列说法正确的是( )
是一种中间产物.下列说法正确的是( )| A. | 1,3丁二烯分子式为C4H8 | |
| B. | 1,3丁二烯转化为 时,先与Cl2发生1,4加成再水解得到 时,先与Cl2发生1,4加成再水解得到 | |
| C. |  在NaOH醇溶液中或浓硫酸存在时加热都能发生消去反应 在NaOH醇溶液中或浓硫酸存在时加热都能发生消去反应 | |
| D. |  催化氧化得X,X能发生银镜反应,则X的结构只有两种 催化氧化得X,X能发生银镜反应,则X的结构只有两种 |
7.已知同一碳原子连有两个羟基不稳定: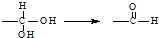 ,下列有关有机物
,下列有关有机物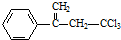 的说法不正确的是( )
的说法不正确的是( )
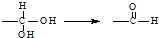 ,下列有关有机物
,下列有关有机物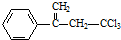 的说法不正确的是( )
的说法不正确的是( )| A. | 属于卤代烃,能使酸性高锰酸钾溶液和溴水褪色 | |
| B. | 该物质存在顺反异构 | |
| C. | 在碱性条件下充分水解,可生成羧酸盐 | |
| D. | 1mol 该物质在一定条件下可与4molH2发生加成反应 |
6.有机物X具有下列性质:①与FeCl3溶液作用发生显色反应;②能发生加成反应;③能与溴水发生反应.依据以上信息,可以得出的推论是( )
| A. | 有机物X是一种芳香烃 | |
| B. | 有机物X可能不含双键结构 | |
| C. | 有机物X不能与Na2CO3 溶液反应 | |
| D. | 有机物X一定含有碳碳双键或碳碳三键 |
2.已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出14种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(5)上表中元素形成的AB型化合物中,离子性最强的是NaF.
| 元素 | H | Li | Be | B | C | O | F |
| X的数值 | 2.20 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| X的数值 | 0.93 | 1.31 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(5)上表中元素形成的AB型化合物中,离子性最强的是NaF.
20. 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
0 168164 168172 168178 168182 168188 168190 168194 168200 168202 168208 168214 168218 168220 168224 168230 168232 168238 168242 168244 168248 168250 168254 168256 168258 168259 168260 168262 168263 168264 168266 168268 168272 168274 168278 168280 168284 168290 168292 168298 168302 168304 168308 168314 168320 168322 168328 168332 168334 168340 168344 168350 168358 203614
 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )| A. | 原子序数:W>Z>X | |
| B. | 气态氢化物的稳定性:N>R | |
| C. | Y和W形成共价化合物 | |
| D. | X和Z两者最高价氧化物对应的水化物能相互反应 |
 ;
;